SOLUTION
検査室支援情報
検査の樹 -復習から明日の芽を-
19 期待が湧くマイクロRNA診断検査
Ⅱ:マイクロRNA診断検査:間近な臨床応用とその課題
はじめに
「Vol.19 Ⅰ:急拡大するマイクロRNA診断検査の基礎」で述べたように、miRNAを筆頭とするncRNAは、諸種疾患群のバイオマーカーや治療薬として、さらには疾患の機構解明などに、その可能性を秘め大きな貢献を果たしている。なかでも本章の主旨であるmiRNAは、1993年に、ビクター・アンブロスとゲイリー・ラブカンの両氏によって発見され、その作用、機能、細胞外形態、応用など広範囲な観点からの機構が解明されて来た。miRNAは、mRNAの3‘UTRを標的としてmRNAを分解または翻訳阻害することで、転写後調節に関与する、18~25塩基ほどの短い内因性非コードの一本鎖RNA分子である。タンパク質をコードするmRNAとは異なり、miRNAはタンパク質合成に関わる遺伝子発現を調節する重要な役割を担っている。
さらに、miRNAは細胞内で遺伝子の翻訳制御に重要な役割を果たすだけでなく、細胞外へ分泌され細胞の外での細胞間コミュニケーションにも関与する。細胞外形態はエクソソームに内包、タンパク質との複合体形成など安定性を保つ合理的な形態で極めて高い安定性が保持されている。エクソソームを介した細胞間でのやりとりはがん細胞でも活発である。また、細胞外miRNAは体液中(血液、尿、母乳など)でも安定しているため、疾患のバイオマーカーとしての研究が活況である。がんを含む多くの疾患における超早期診断や診断が困難な疾患、難儀な鑑別診断などへの応用が期待されている。 疾患としては、がん、神経疾患、心血管疾患、自己免疫疾患、感染症など、様々な疾患での活用が評価されている。
本稿では、間近に迫りつつあるmiRNA診断検査の臨床応用の課題等を集約した。
なお、現況では、測定に関する技術、製品については開発研究が活況であり、商業ペースでの競争も激化しているため技術・製品の個別評価は避け、総論的考察のみにとどめた。
1.期待が湧くマイクロRNA診断検査:そのメリットとデメリット
マイクロRNA(miRNA)は、その固有の安定性と疾患特異性からバイオマーカーおよび診断ツールとして大きな可能性を秘めているが、臨床応用においては、主にアッセイの標準化の遅れが再現性にも影響を与え、実用化への障壁のひとつとなっている。
このため、今ここで、miRNAの実態を調査し、バイオマーカーとしてもしくは疾患診断に用いる意義を確立するためにメリットとデメリットおよび課題とを再考し知識化しておきたい。診断学の歴史的変革期の到来に向け、実用化の到来を待つ事無く、確立に寄与する気概が望まれる。
1.-1) マイクロRNA診断検査:メリット
miRNAをバイオマーカーとして用いるメリットは、早期かつ非侵襲的な診断が可能なこと、治療反応や予後を予測できること、さらに病理診断を終えたホルマリン固定パラフィン包埋(FFPE)組織などの保存サンプルからも測定可能なことなどが挙げられる。デメリットは、測定系を含めた各作業工程の標準化の難しさ、検出と定量の複雑さ、miRNAの他分子からの干渉、大規模なコホート検証研究の必要性が挙げられる。これらを詳細に列記すると、
早期かつ非侵襲的な検出:miRNAは、血清、血漿、尿、唾液など、様々な体液から容易かつ非侵襲的に採取・検出できる。循環miRNAは血液などの体液中から検出できる。
疾患のサブタイプ分類:miRNAの発現パターンは腫瘍のサブタイプを区別するのに役立ち、適切な治療法を選択する上で極めて有用である。
予後予測および予測価値:miRNAレベルは、疾患の進行や治療に応じて動的に変化する可能性があり、治療効果のリアルタイムモニタリングや患者転帰の予測に有用である。
高い安定性:循環miRNAは、エクソソームなどの小胞に封入されているかタンパク質に結合しているため、非常に安定しており、温度変化や凍結融解サイクルなどの過酷な環境下でも酵素分解から保護されている。長年保存されたアーカイブ組織サンプルからも確実に検出が可能である。
高い診断精度:miRNAは、非アルコール性脂肪性肝疾患(NAFLD)などの異なるステージの鑑別など、病態の鑑別において高い診断精度を発揮する。
疾患の早期兆候:miRNA発現プロファイルの変化は、疾患の超早期段階で観察できることが多く、広範囲の疾患に渡って、臨床症状や従来のタンパク質マーカーよりも早期の診断と介入が可能である。
組織および疾患特異性:特異的なmiRNAシグネチャーは、特定の組織、細胞種、および疾患(例えば、特定のがん)に固有のものであり、標的診断、原発不明がんの起源組織の特定、および様々な疾患サブタイプの鑑別に有用である。
技術的感度:定量的逆転写PCR(RT-qPCR)などの標準的な検出技術は高い感度を有し、少量のRNAで微量miRNAの検出と定量が可能である。
などの利点があげられる。
1.-2)マイクロRNA診断検査:デメリット
標準化の欠如:サンプルの採取、取り扱い、保管、抽出、検出、データ解析など、前分析法および分析やデータ処理など一連の標準化プロトコルが構築できていない。このため、研究間でしばしば相反する結果が生じることがある。
検出の複雑さ:miRNAは分子サイズが小さく、高感度な手法が必要となるため、検出と定量は技術的に困難である。また、取り扱い中の分解を防ぐ必要がある。
生物学的干渉:体液中の他の分子がmiRNAの検出と分析に干渉する可能性がある。
血球汚染:血球由来のmiRNAの存在は、miRNAの循環レベルに影響を与える可能性と精度に影響を与える可能性がある。また、血液由来試料は溶血への配慮が不可欠である。
大規模コホート検証の必要性:現在の研究成果のほとんどは小規模なグループでの成果が多い(コホート規模の小ささ)。診断の堅牢性を確認するには、多様な集団や病態における臨床的有用性を確認する大規模かつ独立した臨床試験での検証が必要である。特にmiRNAの多様性や遺伝的背景、(SNP)等の個人差、環境要因と生活習慣、年齢と性別、民族、疾患の進行ステージと腫瘍の異質性などを考慮した大規模コホート検証が不可避である。
機能理解の限定:疾患における多くの miRNA の複雑な役割とメカニズムはまだ完全には解明されておらず、結果の解釈が複雑になる可能性がある。
SNPs、miRNAファミリーの拡大(IsomiRなど)、1つのmiRNAが複数のmRNAの制御に関与、内因性競合など充分には解明されていない生物学的機能が残されている。
一貫性のない結果の発生:特定のmiRNAの発現パターンは、研究方法、サンプルサイズ、患者コホートの違いにより、研究間で大きく異なる場合があり、検証が困難である。
特異性とオフターゲット(本来意図した標的以外に作用する現象)効果:一部のmiRNAは特異性が高い一方で、様々な疾患と関連するため、特異的バイオマーカーとしての使用は限定的である。治療の観点からは、miRNAはオフターゲット効果を持つこともあり、意図しない副作用につながる可能性がある。
低い存在量:関連するmiRNAの中には、循環血中に非常に低いコピー数で存在するものがあり、標準的な方法では正確な検出が困難なためデジタルPCRなどのより高価で複雑な手法が必要となる可能性がある。
高コストとバイオインフォマティクスの課題:次世代シーケンシング法の分析成果は強力で一度に多くの結果を生む反面費用がかさむ。さらに、データ分析と解釈には高度な計算基盤と専門知識が必要である。
1.-3)マイクロRNA診断検査:臨床応用への課題
マイクロRNA診断検査は、諸種の体液や排出液などから非侵襲的に採取され、広範囲な疾患群の早期発見、精度・正確度の高い診断や予後予測など、極めて有益なバイオマーカーとしての期待を秘めており、その臨床応用には高い期待が寄せられている。しかし、その臨床応用には、測定操作・技術・データ解析等の標準化の不備、試料選択、検出精度の向上、生物学的な解釈の複雑さといった複数の課題を残し足踏み状態の現状と云える。
臨床診断へのmiRNA実用化遅れの大きな課題としては、①標準化されたプロトコルの欠如:詳細なプロトコルが標準化されていないため検査室間での結果に一貫性がないことが挙げられる。その他、②多様な集団を対象とした大規模な臨床検証の欠如、様々な影響因子が交錯するmiRNAレベルの生物学的複雑性があげられる。さらに、③新しい診断検査の開発に伴う高コストとPMDA、FDAやEMA、などの規制機関の分子診断検査に定める厳格な品質・安全性の審査基準をクリアするためのデータ作成の多大な労力と投資が必要である。
2.不可避なプロトコルの標準化:なぜの例
標準化されたプロトコルの欠如:miRNAの抽出および定量方法が異なるとばらつきが生じ、研究間や検査室間で結果を比較することが困難となる。
再現性の問題:シーケンシングなどの分析技術はバイアスの影響を受けやすく、他のプラットフォームでは再現性が得られ難い場合もある。また、測定する試料の選択も重要である。
さらに、同じ血漿でも、どの抗凝固剤を用いるかによりサンプルからのばらつきが生じる。採血管(例:クエン酸 vs. EDTA)を例にしても、miR-191-5p、miR-320a、miR-21-5p、miR-23a-3pいずれもクエン酸と比較してEDTA血漿で有意に増加、miR-451aもクエン酸と比較してEDTA血漿で有意に増加し、さらに溶血とも関連する[1]。
尿においても、Grimaldiらは、尿中miRNAに関する現在の最先端の試験を収集し、精選・特定した25件の報告(N=4054名の参加者)を解析した結果、1つの研究で発見されたmiRNAは66個、2つの研究で発見されたmiRNAは15個、3つの研究で発見されたmiRNAは1個であった。25件のうち8件(32%)は全尿、8件(32%)は上清、5件(20%)は尿沈渣、4件(16%)は尿エクソソームに焦点を当てていた。また、特定された同じmiRNAで1つの研究では、アップレギュレーションされ、別の研究ではダウンレギュレーションされたものもあった。結論として、非侵襲的な採取:尿は簡単に採取でき、患者にとっても負担が少ない。安定性:miRNAは分解抵抗性が高く、尿中でも安定して存在する。臓器特異性:尿中のmiRNAは特定の臓器由来のものが多く、例えば腎臓特異的なmiRNAは腎障害の検出に有効である。早期診断:尿中のmiRNAは病気の初期段階でも検出できるため、早期診断に有益であると評価するも、結果の多様性、プロトコルの標準化の必要性とさらなる追加研究の必要性を述べている[2]。
これら報告された結果の多様性については、枚挙に暇が無い。信頼性の高い循環miRNA研究のために標準化されたサンプル収集および処理方法の重要性を浮き彫りにしている。サンプルの種類、処理方法などの小さな要因でも実験結果に大きく影響し、結果に一貫性がなくなる可能性が想定されるためプロトコルの標準化は不可避である。診断に有用な血液中miRNAについては、複数の研究で様々なmiRNAの種類や発現方向(上昇または低下)が一致しないケースが多く報告されているがこれは、標準化だけの問題ではない、次の様な幾つかの要因も考慮すべきである。
研究デザインと手法の違い:サンプル腫およびサンプル収集方法(血清か血漿か)、RNA抽出プロトコル、miRNA検出技術(次世代シーケンシング、マイクロアレイ、リアルタイムPCRなど)、データ解析方法が研究ごとに異なるため、結果にばらつきが生じる。
サンプルの不均一性:前立腺がんなどは非常に不均一な疾患であり、患者の年齢、人種、がんの進行度、悪性度(グリソンスコア)などの臨床的特徴が異なる。また、組織由来のサンプルでは、がん細胞に隣接する正常組織や間質細胞の混入も結果に影響を与える可能性がある。
バイオマーカーとしての特異性と感度の限界:単一のmiRNAマーカーだけでは高い診断精度(特異度と感度)を得ることが難しく、複数のmiRNAを組み合わせたパネル診断が提案されている。
結果の再現性と検証の不足:いくつかの研究で有望な結果が報告されても、他の独立した研究グループによる追試や大規模な検証研究が不足している場合がある。
生物学的複雑性:レベルは、年齢、食事、運動など、多くの要因の影響を受けるため、解釈が困難である。また、その調節機構についてはより深く理解する必要がある。生物学的機構の複雑性としては、miRNAのSNPs[3]やIsomiR[4]、競合的内因性RNA(ceRNA)[5][6]、1つのmiRNAは複数のmRNAを制御する[7]ことの理解・解明も重要である。
さらにはceRNAの機構も重要である。
競合的内因性RNA(competitive endogenous RNA:*ceRNA)
ceRNAの仕組み:このメカニズムは、miRNA、ceRNA、mRNAの3つのRNA分子の相互作用で成り立つ。
*ceRNA:miRNAの「スポンジ」として機能する内因性のRNA分子です。ceRNAは、miRNAが結合するための特定の配列(miRNA応答配列)を持っており、miRNAを「吸着」する。代表的なceRNAには、mRNA、lncRNA、環状RNA(circRNA:環状構造を持つ非コードRNAで、特に強力なmiRNAスポンジとして機能する)がある。
競合的内因性RNA(ceRNA)ネットワーク:ceRNAの概念は、以下のような「ネットワーク」として働く。細胞内に存在するさまざまなceRNA(mRNA、lncRNA、circRNAなど)が、共通のmiRNAを巡って競合する。あるceRNAの量が増加すると、より多くのmiRNAを吸着する。その結果、他の標的mRNAに結合できるmiRNAの量が減少し、標的mRNAからのタンパク質合成が促進される。逆に、あるceRNAの量が減少すると、遊離したmiRNAが増加し、他の標的mRNAの発現をより強く抑制する。このように、ceRNAネットワークは、miRNAを介した間接的な経路を通じて、細胞内の多数の遺伝子発現を調節する。
生物学的意義:ネットワークは、さまざまな生物学的プロセスにおいて重要な役割を果たしていることが示されている。
疾患への関与:がん(卵巣明細胞癌、骨肉腫など)やアルツハイマー病といった多くの疾患において、ceRNAネットワークの異常が病態に関与していることが明らかになっている。
バイオマーカー:これらのネットワークの異常は、疾患の診断や予後予測のための新しいバイオマーカーの候補として注目されている。
遺伝子治療:ネットワークを標的とした遺伝子治療の可能性も探索されている。
3.課題は残されているがそれでも着実に成果が・・・マイクロRNA診断検査
マイクロRNAバイオマーカーは、基礎研究では魅力的な膨大な量のデータが蓄積されているが、これまで述べた幾つもの課題を残しており、研究から臨床への展開は遅れている。特に血液を中心とする試料分野はその傾向が顕著である。この様ななかにおいて尿を試料とするmiRNAは着実に臨床応用を成しつつある。尿中のmiRNAは非侵襲的で簡便に採取でき、血液と比較し、構成成分の少なさ、含まれる細胞の種類が限定的な点等が優位に作用するのかも知れない。尿の測定では、すい臓がんの早期発見や薬剤誘発性腎障害の検出、膀胱がん検出などに成果を挙げている。臓器特異的なmiRNAがバイオマーカーとしての役割を果たすことが期待されている。
これまでは困難であった骨軟部腫瘍の良性・悪性を鑑別するバイオマーカーとして、いくつかのmiRNAが悪性骨軟部腫瘍の診断や予後予測に有用であることが示されている。miR-21、miR-31、miR-199a、miR-146b、miR-345:これらのmiRNAは、悪性腫瘍組織において良性腫瘍組織と比較して有意に高発現している。miR-199a:血清サンプルでも悪性群で高発現、miR-30e:悪性腫瘍群の血漿サンプルで高発現、7種のmiRNAからなる診断指標 (Index VI):国立がん研究センターの研究により同定された、悪性骨軟部腫瘍の診断に非常に高い精度(感度90%、特異度95%)を持つ指標である。この7種の具体的なmiRNA名は文献中では明示されていないが、これらを組み合わせることで、組織型によらず悪性腫瘍を識別できるとされている[8][9]。
PBMNC「末梢血単核細胞」中のmiR-181b-5p、miR-21-5p、miR-195-5p、miR-137、miR-346、およびmiR-34a-5pは、統合失調症において高い診断感度と特異度を示すことが明らかになり、結論として、血液由来miRNAは統合失調症診断の有望なバイオマーカーとなる可能性があると報告された[10]。
また、少量の血液により早期乳がんを検出し、乳腺の良性病変との鑑別ができるようになった[11][12]。
悪性度が非常に高いが診断が困難でありかつ効果的な早期発見法が欠如していたすい臓がんにおいて、尿中マイクロRNAと機械学習との併用により、92.9%という検出感度で早期から末期まで診断可能な手法が報告された[13]。さらに、食道がん、乳がん、肺がん、胃がん、大腸がん、膀胱がん、腎臓がん、卵巣がん、前立腺がんおよび膵臓がんを加えた10種のがん診断を尿中マイクロRNAで診断する商業ベースの診断検査がスタートしている。
この様に、これまでは診断が困難であった疾患の診断や重要な鑑別診断がmiRNA等のncRNAと機械学習との併用により比較的容易にかつ超早期診断が可能となりつつある。
4.マイクロRNA:疾患診断への応用例
4.-1)心血管疾患
アテローム性動脈硬化症は、プラークの蓄積により動脈内が狭くなる疾患で、無症状の期間が長く、慢性の進行性炎症性疾患である。病状が進行すると、影響を受ける動脈箇所により、脳卒中、心筋梗塞、不安定狭心症などを発症し、稀には致命的な急性心血管イベントにつながる可能性がある。このため早期に無症状期の潜在性動脈硬化症患者を探知することは重要な課題である。このため、早期検出のバイオマーカーとしてmiRNAが着目されている。
多様な早期大動脈弁狭窄症診断にmiRNAを導入するに際しては、診断目的や被験者の病態によりmiRNAの選択も異なる可能性もある。例として3篇の論文を提示する。
Ghafouri-Fardら[14]は、 冠動脈疾患(CAD:Coronary Artery Disease)において、マイクロ RNA (miRNA) は、内皮細胞の増殖とアポトーシスの調節、免疫反応の誘導、プラーク形成のさまざまな段階に関係している。CAD 患者では、miR-92a-3p、miR-206、miR-216a、miR-574-5p、miR-23a、miR-499、miR-451、miR-21、miR-146a、およびその他の多数の miRNA のアップレギュレーションが報告されている。また、対照的に、miR-20、miR-107、miR-330、miR-383-3p、miR-939、miR-4306、miR-181a-5p、miR-218、miR-376a-3p、および miR-3614 は、CAD でダウンレギュレーションする miRNA の一部である。このため、CAD 患者における miRNA の差次的発現は、CAD 患者を評価するための診断パネルまたは予後パネルの設計に利用されてきた。
さらに、ルシフェラーゼレポーターアッセイにより、多数のmiRNAとmRNA間の機能的相互作用を示している [15][16]。 miRNAは、
血管新生の調節 miR-92a-3p[17]、miR-939[18]、miR-206[19]、
炎症反応 miR-181a-5p、miR-181a-3p[20]、miR-216a[21]、miR-383-3p[22]、
白血球接着 miR-21[23]、miR-25[24]、
*VSMCの活性の調節 miR-574-5p[25]、
*vascular smooth muscle cell:血管平滑筋細胞
など、さまざまなメカニズムを通じてCADの発症を制御することができる。
たとえば、miR-206 は、血管新生プロセスに関与する VEGF、PIK3C2α、Akt、および内皮型一酸化窒素合成酵素の発現を制御する。
NF-Kβ/TNF-α、PI3K-Akt-mTOR、WNT、および VEGFA/ERK1/2/NF-κB は、CAD のコンテキストで miRNA によって制御されるシグナル伝達経路の一部である。
Witartoら[26]は、潜在性頸動脈アテローム性動脈硬化症の診断バイオマーカーとしての血液中の循環マイクロRNAを評価した。11 種類の miRNA(miR-18a-5p、miR-29a、miR-29b、miR-29c、miR-146a、miR-183-5p、miR-186-5p、miR-192-5p、miR-374、miR-488、miR-675-3p)は、潜在性臨床的頸動脈アテローム性動脈硬化症患者で発現が上昇し、4 種類の miRNA(miR-199a-3p、miR-211-5p、miR-532-5p、miR-637)は低下した。すべての研究で、循環 miRNA と CIMT(頸動脈内膜肥厚)の間に有意な相関関係が報告された。
循環 miRNA の診断精度は研究間でばらつきがあり、miR-675-3p が最も高く、miR-29a が最も低かった。miRNAのCIMT診断における有益性が高く評価された。
Hanら[27]は、アテローム性動脈硬化症(AS:Aortic Stenosis)を2つのmiRNAに基づく指標を評価した。
WGCNA:an R package for weighted correlation network analysis:加重遺伝子共発現ネットワーク解析(Langfelder, P. et al. BMC Bioinformatics 9, 559 (2008).)
WGCNAにより、ASと有意に相関する42個のmiRNAと532個の遺伝子を明らかにし、諸種の解析を加え、最終的にhsa-miR-654-5p、hsa-miR-409-3p、hsa-miR-485-5p、hsa-miR-654-3pの4個のmiRNAをASの潜在的に重要なバイオマーカーであることを特定した。結論として、本研究では、hsa-miR-654-5pとhsa-miR-409-3pを含む合計2つのmiRNAがASの潜在的に重要なバイオマーカーとして特定され、特定された2つのmiRNAに基づくロジスティック回帰モデルは、AS患者を正常な症例と確実に区別することができた。
4.-2)がんにおけるマイクロRNA
『miRNAは、がん[28]、心血管疾患[29]、神経変性疾患[30]、精神疾患[31]、慢性炎症性疾患[32]などの発症と進行に関わっている[33]。特に、がんの原因因子についてはさまざまな議論がなされているが[34]、その中でもmiRNAは、細胞のがん化に深く関与していることが多くの研究者らによって指摘されている[35][36][37]。
miRNAとがん化の関わりについて、2002年、米国のG. M. CalinとC. M. Croceらによって最初の報告がなされた[38]。
それ以降、がんに関わるmiRNAに、正の制御をする(がん化を促進する)ものと負の制御をする(がん化を抑制する)ものの2種類のタイプが存在することがわかった[39]。
正の制御をするmiRNAはonco miRNA(oncogenic miRNA, がん促進型miRNA)[40]、負の制御をするmiRNAはTumor Suppressor miRNA(がん抑制型miRNA)[41]と呼ばれている[42][43]。 特に、onco miRNAに関して、その発現量の亢進が細胞のがん化を誘発していることが明らかにされている[44]。つまり、miRNAの発現量異常は、生物の恒常性の破綻に直結する。
代表的なonco miRNAとtumor suppressor miRNAには
- 〇 miR-21:onco miRNA
- 乳がん[45]、子宮頸がん[46]、肺がん[47]、大腸がん[48]など
- 〇 miR-34:tumor suppressor miRNA
- 前立腺がん[49]、肺がん[50]、大腸がん[51]、肝臓がん[52]などがある。
2010年、米国の研究グループは初期のリンパ腫を人為的に発症させたトランスジェニックマウスを作製した[53]。そのマウスにおいて、onco miRNAのひとつであるmiR-21 (miRNA-21)というmiRNAの発現量を抑制した場合、プレB細胞由来のリンパ腫の消滅が観察された。そのため、onco miRNAの発現量を低下させ、がん細胞を消滅させるという方法は、がんの新たな治療薬の開発手法のひとつとして注目されている[54][55][56][57]。
事実、miRNAとがん発症に高い相関性が見られることから、がんを中心としたさまざまなヒト疾患に対する核酸医薬品の開発が盛んに行われている。
2013年、米国の研究グループによって、miRNA mimic(miR-34a mimic)をがん患者に投与した、最初の臨床研究がはじまった[58]。以降、2015年までに米国では数十例の臨床研究が進められてきた[59]。また、マイクロRNAについてはがん診断のためのバイオマーカーへの応用も期待されている[60][61][62][63]。
その一方で組織特異性については:一部のmiRNAは組織によって異なる役割を果たす可能性があるため、組織特異的なバイオマーカーとして使用するには慎重な解析が必要である。miRNA - Wikipediaより和訳し引用』
特定のmiRNAプロファイルは、がん、心血管疾患、神経変性疾患、代謝性疾患などのバイオマーカーとして研究されている。miRNAは、標的遺伝子の発現を制御することで、がん細胞の増殖や転移に関与する。しかし、miRNAは、がんの種類や置かれている細胞の状況により、がん促進にもがん抑制にも働きうるため、その機能は複雑である。
- ① がん抑制miRNAの発現低下
正常な細胞では多く発現しているが、がん細胞では発現量が低下するmiRNAがある。これらは、がん細胞の増殖を抑える働きを持つ「がん抑制miRNA」と考えられている。
miR-145:大腸がん、前立腺がん、膀胱がんなどで分泌量が減少し、がん抑制因子として機能する。正常な細胞では細胞増殖を抑制するが、がん細胞では発現が低下することで、がん細胞の増殖を促す。
miR-200ファミリー:5つのメンバー(miR-200a、miR-200b、miR-200c、miR-141、miR-429)から構成されるmiRNAの一群である。これらは、細胞の分化、癌の発生・転移、上皮間葉転換(EMT)など、重要な生命現象の調節に関与する[64]。
miR-200ファミリーは、上皮間葉転換EMTの重要な抑制因子として機能する。ZEB1やZEB2といったEMT誘導転写因子を直接標的とし、それらの発現を抑制することで、上皮細胞の表現型を維持し、癌細胞の移動や浸潤を妨げる。
肺がん、卵巣がん、腎臓がん、乳がん、膀胱がんなど、多くの癌種において、miR-200ファミリーの発現低下が確認されている。発現が低下すると癌の進行や転移が促進されることから、癌抑制遺伝子として働くと考えられている。標的遺伝子としては ZEB1、ZEB2以外にも、PTENやCRKLなど、細胞増殖やシグナル伝達に関わる複数の遺伝子を標的とすることが知られている循環miR-200ファミリーマイクロRNAが子宮内膜症患者の血漿レベルで変化することや、肺癌におけるPD-L1レベルと相関があることなどから、疾患の診断バイオマーカーや新たな治療標的として研究されている。p53との関連:がん抑制遺伝子p53によって転写活性化され、発現が上昇することが報告されており、p53を介した腫瘍抑制経路の一部を構成していると考えられている。 これらの機能により、miR-200ファミリーは癌研究において特に注目されているmiRNAの一つである[65]。
しかし、がんの種類によってはがん促進的に働くという報告もあり多面性を示す。
miR-205:特に前立腺がんにおいて、がん抑制効果を持つマイクロRNAの一種です。上皮間葉転換を抑制し、細胞の遊走・浸潤を減少させることで、その効果を発揮する。これは、タンパク質キナーゼCイプシロンのダウンレギュレーションによる。また、miR-205は、プロモーター領域の特定の部位をターゲットにすることで、転写レベルでがん抑制遺伝子の発現を活性化することが示されている[66]。
miR-145:様々な生物学的プロセスを制御するマイクロRNAの一種。特に、平滑筋の分化促進、幹細胞の多能性抑制、がんの増殖や転移抑制などの機能を持つことが知られている。がんにおいては、多くの種類のがんで発現が低下し、腫瘍抑制因子として働くため、がんの診断マーカーや治療標的としての可能性が期待される[67]。
miR-15/miR-16:B細胞性慢性リンパ性白血病(CLL)では、これらのmiRNAの遺伝子座(13q14)が欠失していることが多く、発現が低下している。
miR-16:慢性リンパ性白血病(CLL)で高頻度に発現が低下し、がん抑制遺伝子として機能することが示されている。
miR-34a:腫瘍抑制因子として知られ、p53経路の下流でがん細胞の増殖抑制やアポトーシス誘導に関わる。
miR-874:乳がん細胞の増殖を抑制するメカニズムが報告されている。
miR-223:腫瘍抑制因子として機能する。CLL患者では発現が低下しており、予後不良と関連する。特に、IgVH非変異型やZAP70高発現の患者で発現が低いことが報告されている。 -
② がん促進miRNA(オンコmiRNA)の発現増加
がん細胞で発現量が増加し、細胞の増殖や生存を助けるmiRNAもある。これらは「オンコmiRNA」と呼ばれる。
miR-21:膵臓がん、乳がん、大腸がん、肺がんなどで高発現する。miR-21は、がん細胞の増殖を促進したり、化学療法への耐性を高めたりする。細胞内では、他の遺伝子の発現を翻訳抑制やmRNA切断などのメカニズムで調節する重要な役割を担っている。
miR-21の主な機能と役割としては、遺伝子発現制御、細胞の分化、増殖、アポトーシスといった生命現象に深く関与している。悪性腫瘍で高発現していることが多く、癌抑制因子であるPDCD4、PTEN、SPRY2などの翻訳を直接抑制し、癌細胞の増殖や悪性化を促進させる「癌原遺伝子(OncomiR):オンコミル」として知られている。がん(食道がん、胃がん、肺がん、大腸がん、乳がん、膵がんなど)だけでなく、炎症性腸疾患や心臓病、自己免疫性膵炎などの様々な疾患との関連が研究されている。
バイオマーカーとしての可能性は、様々な疾患の診断や予後予測に期待されている。乳がんや大腸がんなどでは、血清中のmiR-21レベルが健常者に比して高い、さらに病期の進行に伴って上昇することが報告されている。治療標的として、 miR-21の働きを阻害する、がん治療や急性炎症性肺疾患などの新たな治療戦略も研究されている。
miR-21は、医学研究において非常に注目されているmiRNA分子である[68]。
miR-10b:乳がん細胞で発現が亢進し、転移を促進する働きがある。
miR-17-92クラスター:遺伝子を抑制することで、がん細胞のアポトーシスを回避させ、無限の増殖能力を促進する[69]。
*miR-17-92クラスターとは、ゲノム上の特定の領域から同時に転写される、6種類のマイクロRNA(miR-17、miR-18a、miR-19a、miR-20a、miR-19b、miR-92)がクラスターを形成したものである。これらはそれぞれ異なる標的遺伝子の翻訳を抑制することで、細胞増殖、分化、アポトーシスなど多くの細胞機能に影響を与え、がんの発生や進行に深く関与することが知られておりがん遺伝子として機能することがある
miR-155:子宮頸がんや胆嚢がん、膵臓がんなどで分泌量が増加し、予後不良との関連が報告されている。細胞の増殖や、他の細胞とのコミュニケーションを介して転移を促進する[70]。
miR-210:様々ながんで発現が増加し、血管新生を促進する。 -
③ がん細胞から分泌されるmiRNAの働き
がん細胞から分泌されるmiRNAは、細胞間の情報伝達物質として機能し、周囲の正常細胞や離れた組織の細胞の性質を変化させることで、がんの悪性化(増殖、浸潤、転移)の促進や免疫応答の抑制に関与する[71]。
免疫抑制:がん細胞は、エクソソームを介して特定のmiRNA(例:miR-214)を分泌し、免疫細胞(制御性T細胞)に取り込ませる。これにより免疫細胞の機能を抑制し、がん細胞が免疫系から逃れるのを助ける。
線維芽細胞への作用:がん細胞から分泌されたmiRNAが、正常な線維芽細胞に取り込まれ、がん関連線維芽細胞のような形質に変化させることがある。 -
④ 同じ臓器に発生したがんでもその種類やサブタイプによってマイクロRNA (miRNA) の発現パターンは異なる[72]
マイクロRNAの発現パターンは、がんの種類によっても異なる。
肺がん:喫煙者や非喫煙者のがん細胞で異なるmiRNAプロファイルが見られる。また、非小細胞肺がん(NSCLC)と小細胞肺がん(SCLC)でも異なる発現パターンが確認される。let-7は非小細胞肺がんでは発現の低下が報告されている。let-7の発現低下は予後不良と関連しており、特に腺がんなどで顕著に見られる[73]。
乳がん:分子サブタイプ〔ルミナルA型、ルミナルB型(HER陽性)、(HER2陽性型)、(トリプルネガティブ乳がん (HR陰性、HER2陰性) 〕によって、発現するmiRNAの種類や量が異なる。 -
⑤ マイクロRNAの放出
これらのマイクロRNAは、エクソソームに抱合、もしくはタンパク質と結合して細胞外へ放出される。がん細胞由来のエクソソームは、正常細胞のエクソソームとは異なるmiRNAを運ぶことで、がん細胞と周囲細胞間のコミュニケーションに影響を与え、がんの進行に関与すると考えられる。 -
⑥ miRNAの臨床応用
このようなmiRNAの発現パターンの違いは、がんの早期発見や診断に用いられる。
血液検査:がんの種類によって血液中のエクソソームに含まれるmiRNAの種類や量が異なることを利用して、血液サンプルから特定のがんを検出する研究や実用化が進められている。
尿検査:尿中に含まれるmiRNAを調べることで、すい臓がんなどの早期発見を目指す検査も開発されている。
4.-3)がん以外のマイクロRNA診断が有効な疾患名と具体的なマイクロRNA
マイクロRNAは、がん、心血管疾患、神経変性疾患など多くの疾患の診断に用いられる。
心血管疾患に対する:miR-16、
miR-16は心血管疾患(CVD)において複雑な役割を果たしており、異なる形態が相反する作用を示す。miR-16-5pはアポトーシスと酸化ストレスを促進することで転帰を悪化させる可能性を示唆する研究がある一方で、miR-16-2-3pは血管機能を改善することで保護作用を示す可能性を示唆する研究もある。しかし、どちらも潜在的な診断バイオマーカーおよび治療標的として研究されている。
心筋梗塞(MI):虚血性心筋症患者の血漿中のmiR-16-5pレベルは上昇しており、心筋細胞における*ERストレス誘発性のアポトーシスと酸化ストレスを促進する可能性がある。
*ERストレスとは、細胞小器官である小胞体(ER)内部に、折りたたみの不全なタンパク質や異常なタンパク質が蓄積した状態を指す。これは、細胞内外からの様々なストレス(飢餓、低酸素、酸化ストレス、カルシウム濃度の変化、ウイルス感染など)によって小胞体の機能が障害されることで発生する。
*ATF6などの遺伝子を標的とすることで、miR-16-5pはERストレスの増加と心臓損傷を引き起こす可能性がある。
*ATF6とは、細胞内の小胞体ストレス応答において中心的な役割を果たす膜結合性の転写因子。
心筋梗塞の増悪:miR-16はインスリン受容体基質1(IRS1)を標的とし、アポトーシスと血管新生を誘導することで、心筋梗塞の障害を増悪させる可能性がある。miR-16-5pのベースライン発現が低い場合、血栓症関連の循環血中miR-16-5pを有する患者では入院期間が長くなる。miR-16-2-3pの潜在的な保護的役割としては、冠動脈微小血管機能障害:循環エクソソームmiR-16-2-3pは冠動脈微小血管機能障害と関連しており、その過剰発現は心機能を改善する可能性がある。メカニズム:miR-16-2-3pは、内皮細胞における脂肪酸分解を制御し、細胞遊走と管腔形成を促進する。特定のmiR-16アイソフォームのレベルは、リスク評価、疾患進行のモニタリング、および転帰予測の診断バイオマーカーとして使用される[73][74]。
・心不全の潜在的な治療戦略に用いられる:miR-92
その他の疾患としては、
多発性硬化症(MS)などの神経疾患に対するmiR-124およびmiR-146aなど[75]
肝疾患に対する:miR-122[76]、
肝臓特異的で、C型ウイルス性肝炎や非アルコール性脂肪性肝疾患(NAFLD)などの肝疾患の診断に用いられます。
- ・NAFLD(非アルコール性脂肪性肝疾患)および非アルコール性脂肪性肝炎(NASH)と関連:miR-192
- ・NAFLDおよびNASH患者で増加:miR-34a、miR-21
- ・乾癬病態に関与する乾癬特異的なマイクロRNA:miR-203[77]
- ・多発性硬化症(MS)の病態と関連:miR-124
- ・MS患者に認められ、予後予測バイオマーカー:miR-146a
- ・パーキンソン病(PD)における炎症に関与し、健常者と区別する:miR-7–1–5pおよびmiR-223–3p
- ・B型およびC型肝炎ウイルス感染と関連:miR-122、miR-155
- ・インフルエンザウイルスと関連:miR-21およびmiR-223
- ・喘息の重症度および季節性症状と関連:miR-328-3pおよびlet-7d-3p
その他、多くの疾患において研究が進行している。
4.-4)複雑な特定の疾患の診断には、複数のmiRNAの組み合わせが有用
特定の疾患、特にがんや心血管疾患などの複雑な疾患の診断においては、単一のmicroRNAではなく、複数のmiRNAの組み合わせ(パネル)が、診断精度と特異性の向上に有効である。これに機械学習・AIとを併用することによりより一層の成果が期待される。
miRNAパネルは、病気の複雑な生物学的プロセスをより包括的に捉えることができ、単独のバイオマーカーよりも優れた有効性を発揮する。特に数種の限定疾患の鑑別診断だけではなく多種類のがん診断には多数のmiRNAを使用しないと高い成果は得難いと云われている。以下に、研究段階または臨床応用間際の特定の疾患向けmiRNAパネルの例を示す。
がん診断のためのマイクロRNAパネル
がん診断研究においては、血液(血清や血漿)中のmiRNAの組み合わせを機械学習で解析し、がんの種類や早期発見の可能性を検討する「多がん早期検出(MCED)検査」の開発が進んでいる。
血中マイクロRNAによって13種のがんを高精度に区別できることを実証
〔血中マイクロRNAによって13種のがんを高精度に区別できることを実証|国立がん研究センター〕
わが国において、大規模な血清miRNomicsと機械学習を組合せた、血液ベースのがん分類システムの開発が進展中である。『トレーニングセットは13種類の固形がんの患者からの7931個の血清サンプルと5013個の非がんサンプルで構成され、検証セットは1990個のがんサンプルと1256個の非がんサンプルで実施された。結果、がんの種類は、全てのステージで0.88(95% 信頼区間 [CI]=0.87~0.90)の精度で予測され、ステージ 0~Ⅱでは0.90(95% CI=0.88~0.91)の精度で予測された。13種類のがんの判別に関するF1スコアは0.93であった。がんの種類の正確な予測には最も大きく貢献したmiRNAが少なくとも100個ある場合、最適な分類性能が達成されたと報告されている。本結果より、miRNAを使用してがんの種類に特異的な血清miRNomeを確立できることを示唆している。JNCI Cancer Spectr. 2023 Jan 3;7(1):pkac080. Abstractを和訳し引用[78]。』
日本の国立がん研究センターなどの研究グループは、乳がん、大腸がん、肺がん、胃がん、膵がんなど13種類の固形がんを対象とした大規模研究結果を発表した。
複数のmiRNAの血中濃度パターンを機械学習で解析することにより、高い精度でがんの種類を予測できる診断モデルを構築した。特に、食道がんでは、特定のmiRNAの組み合わせによりステージ0から高い感度で検出可能な診断モデルが報告されている(感度96%、特異度98%)。この研究では、成果として具体的なmiRNAデータと解析コードが公開され、今後の実用化に向けた検証が進んでいる。
大腸がん(CRC):miR-106b-5p、miR-1246、miR-16、miR-21-5pなどの組み合わせを含むパネルが、高い診断精度(AUC約0.9)を示している。血清由来のmiRNAパネルは、早期スクリーニングのための強力なバイオマーカーとして期待されている[79]。
肺がん:4つ以上のmiRNAの組み合わせが、単独のmiRNAよりも高い診断精度(感度90%、特異度93%、AUC 0.97)を示した。
非小細胞肺がん(NSCLC)の早期発見のための4-miRNAパネル (miR-150-5p、miR-301b-3p、miR-369-3p、miR-497-5p
) が提案された[80]。
肝細胞がん(HCC):hsa-miR-221とhsa-miR-29cの組み合わせが、個々のmiRNAよりも効果的で安定した診断精度を示すことが報告された[81]。
前立腺がん:miR-106b-5p、miR-129-1-3p、miR-381-3pの3-miRNAパネルが高い診断能(AUC 0.912)を示した[82]。
乳がん:let-7b-5p、miR-122-5p、miR-146b-5p、miR-210-3p、miR-215-5pの5-miRNAパネルが、血漿中の新規非侵襲的バイオマーカーとして同定された[83]。
心血管疾患(CVD)向けmiRNAパネルCVDにおいても、miRNAは潜在的なバイオマーカーとして研究されており、特に急性心筋梗塞(AMI)などの診断において、既存のバイオマーカー(トロポニンなど)を補完または上回る可能性がある[84][85]。
冠動脈疾患(CAD):miR-17、miR-126、miR-92a、miR-145、miR-155などの複数のmiRNA発現低下が確認された。
miR-132、miR-150、miR-186の3-miRNAパネルは、不安定狭心症の診断において、従来のバイオマーカーよりも高い精度を達成した。
miR-423を含むパネルは、従来の心血管リスク因子に基づくモデルに加えて、診断性能を向上させることが示された。
急性心筋梗塞(AMI):心筋特異的miRNAである miR-1、miR-133a、miR-208、miR-499 は、心筋梗塞後の循環血中で増加する。miR-1291、miR-217、miR-455-3p、miR-566の4-miRNAパネルは、AMIの早期診断ツールとして有望であることが特定された。
臨床診断ツール: Mets パネルは、癌の原発巣不明転移を特定するマイクロRNA(miRNA)ベースの診断アッセイツールです。Rosetta Genomics社によって開発され2012年に発売されたが、2018年に会社が破産し、現在の製品の入手性や状況は不明である。64種類のmiRNAの発現レベルを測定し、既知の42種類の異なる腫瘍タイプと照合する。バリデーションサンプルセットにおいて、90%の精度で原発巣を同定し、患者の臨床病理学的評価と88%の一致を示したと報告。miRNAを利用した診断ツールの先駆けの一つとして臨床応用された製品である。
マイクロRNA(miRNA)パネルを用いた診断は有望性が高い。複数のmiRNAを組み合わせることで、単一のmiRNAよりも正確な結果が得られることが多い。この事はがんのみでなく、神経疾患、心血管疾患、その他の疾患においても同様の傾向が見られる。
5.マイクロRNA検査の実際
5.-1)血液細胞が発現する主なmiRNA
miRNA循環miRNAを分析するための既存の技術のほとんどは、RNA抽出、精製、および小さなRNAの濃縮を伴うため、循環miRNAが部分的に失われ、低濃度miRNAの検出が妨げられる可能性がある。さらに、定量的ポリメラーゼ連鎖反応(qPCR)やドロップレットデジタル(dd)PCRなどの方法で実行する必要がある逆転写ステップは、ターゲットの定量化に影響を与える可能性がある。そのため、これらのステップを回避する直接検出方法の開発が求められている。
この様に有用なバイオマーカーと目されるmiRNAは、組織、血液、血漿、血清、尿、唾液、涙液、精液、母乳など多くの生体試料に存在し測定可能である。しかし、それぞれの試料は固有の特性があり、ただ測るだけでは目的を達しきれないことが多い。例えば、高頻度に測定される血液、血漿、血清においても、正常時、血液を構成する成分は、血漿、赤血球、血栓球、単球、好中球、好酸球、好塩基球、ナチュラルキラー細胞、CD4+T細胞、CD8+T細胞などの細胞が混在しており、かつ混在比も異なる。また、各細胞崩壊に伴う成分放出も試料毎に異なる可能性がある。
血液細胞内のmiRNAのレベルは、発達、老化、および疾患への反応中に変化することがある[87]。血液細胞が発現する主なmiRNAは、
赤血球
• miR-451:RBCで最も豊富なmiRNAの1つであるmiR-451は、顆粒球よりも赤血球において高いレベルで発現している。血漿中にも高濃度含まれており、溶血のバイオマーカーとしても有用である。赤血球の成熟と産生に不可欠な事が示されている。
• miR-144:miR-144は、ヒトおよびマウスのゲノムでmiR-451と密接に関連しており、どちらも赤血球分化を促進する[88]。miR-451/144クラスターとして知られている。
• miR-486:miR-486は、GATA1およびGATA1sと連携して赤血球生成を制御する。
• miR-4732-3p:このmiRNAは赤血球に豊富に存在し、赤血球生成に関与するTGF-β経路の成分を標的にする。
• miR-196a:このmiRNAは、保存中の赤血球の損傷に関連する。
• miR-142:このmiRNAは赤血球の生存を制御する[89]。
赤血球以外の血液細胞(白血球および血小板)で発現する主なマイクロRNA(miRNA)には、miR-223、miR-150、let-7ファミリーメンバー(特にlet-7c)、miR-126、およびmiR-21が含まれる。
白血球
単球、リンパ球、好中球を含む白血球は、それぞれ異なるmiRNAプロファイルを有します。主要なmiRNAとその役割は、以下の通りである。
• miR-223:骨髄細胞(単球および好中球)に豊富に存在し、それらの分化と機能に関与し、血漿中濃度は白血球数と相関する。
• miR-150:リンパ系細胞(T細胞、B細胞、NK細胞)で高発現し、B細胞の成熟と分化に関与する。また、免疫細胞においてアポトーシス促進作用が報告されており、血漿中濃度は対応する血球数と相関する。
• miR-126:白血球および内皮細胞に存在し、循環血中濃度は白血球数および血小板数と有意に相関する。
• let-7a:骨髄系細胞およびリンパ系細胞で発現し、血漿中濃度は白血球数と相関する。
• miR-155:免疫細胞において状況依存的に役割を果たす二重機能miRNAであり、B細胞の成熟および免疫応答に関与する。
• miR-34a:他のmiRNAと同様に、miR-34aは複数のmRNA分子と結合し、それらの遺伝子発現を低下させる役割を担っている。
血小板
血小板は無核ですが、巨核球由来のmiRNAの重要な機能プールを含んでいる。
• miR-223:ヒト血小板に非常に豊富に存在することが一貫して報告されている。
• let-7ファミリー:血小板miRNAの大部分を占め、特にlet-7cが豊富である。
• miR-126、miR-21、miR-24、miR-197:これらも血小板miRNAの中で最も豊富に含まれている。血小板miRNAは微小小胞を介して他の細胞に移行し、血管新生や炎症などの機能に影響する[90]。
この様に血液は幾つもの血液細胞を含み数量的にも多彩である。これに疾患に起因したmiRNAが加わるとさらに多様化することが想定される。この事からも、人間だけの頭脳では解析困難な事象であることが理解できる。
溶血の影響
赤血球の分解(溶血)により、血漿中の特定のmiRNA量が大きく増加することがある。これは赤血球の崩壊に伴い、赤血球中のmiRNAが放出されたことに起因するものである。このため、影響の度合いは溶血の度合いに比例して大きくなる。これによりmiRNAレベルを正確に測定することが困難になることもある。miRNAの測定においては、溶血は色調的影響では無いことを念頭に置いておく必要がある。
溶血により、miR-16やmiR-451などの特定のmiRNAレベルが上昇することがある。
Let-7a、miR-15a,miR21など一部のmiRNAは溶血が有っても比較的安定している。
溶血の有無・度合いは、414nmでの吸光度、溶血比、HスコアまたはHarboe法を使用して評価できる。
溶血の影響を受けやすい microRNA のいくつか(例:miRs-21、-106a、-92a、-17、-16) は、以前にも疾患の血漿/血清バイオマーカーとして提案されており、循環microRNAの測定に使用する血漿/血清サンプルの厳格な品質管理の重要性を強調している。低レベルの溶血は血漿/血清の採取中に頻繁に発生するため、候補となる循環マイクロRNAの測定ではこれを充分に考慮しておくべきである[91]。
5.-2)miRNAの抽出・精製
Kimらは、全RNA調製物と短いRNA調製物のmiRNAデータとは直接比較できない可能性を指摘した。さらに、大きなRNAは小さなRNAのキャリアとして機能する可能性があることを示唆した[92]。
Brownらは、特定のキット間の大きな相違を考慮すると、研究者はより堅牢な抽出方法を選択する必要があり、組織からのmiRNAの量と品質の一貫性と高い回収率を得るには、フェノール:クロロホルム相分離とシリカカラムを用いた固体抽出法(miRVana microRNA isolation)の組み合わせが望ましいと結論付けた。また、組織サンプルからのmiRNA解析には適さない方法(Bioline Isolate II)も特定した[93]。
Lederer らは、miRNeasy、Universal、Trizol、RNeasy、mirVanaキットを比較検討した。miRNA発現分析は、miRNAのサブセットに対してTaqManまたはSYBR Green qRT-PCRを使用した。標準化には外部からスパイクインしたcel-miR-39を使用した。ほとんどの方法は、全RNA濃度と純度の点で同様のパフォーマンスを示した[94]。外部添加したcel-miR-39 と内因性miRNA(RNU6b、miR-16、miR-21)は、さまざまなRNA分離方法間で同等の濃度を示したが、RNeasyミニキットでは一貫して低い値が得られた。
Brunet-Vegaらは、大腸がん患者の血漿からのmiRNA抽出では比較した抽出キットで同等の結果が得られたと報告[95]。一方、Urbizu らは、唾液サンプルに対してはmirVanaキットが最適な抽出結果を示した[96]。Schindlerらは、同様に、腹水中のmiRNA分析に対するmiRNeasy、mirVana、およびTRIzolキットの評価では、miRNeasyキットとmirVana キットが最も信頼性の高い結果を提供し、TRIzolベースの抽出は腹水中のmiRNAに特定の変化をもたらすことが実証された [97]。Bhatiらの研究では、mirVana、miRNeasy、TRIzol法は糞便サンプルでも同様に優れた結果を示したと報告した。磁化固相抽出の新しい方法は、DNA抽出に有望であり、将来的にはmiRNAの分離にも役立つ可能性がある[98]。より正確なmiRNAの決定を可能にする代替アプローチが提供される可能性がある[ 99]。
Wrightらは、羊血漿を用いてmiRNA の分離と定量化の方法を比較した。結果、少量の新鮮および凍結ヒツジ血漿からmiRNAを分離するにはキットmiRNeasy Serum/Plasma kitが最適であり、miRNA検出と操作要因を考慮するとmiRNeasy Serum/Plasma Advanced kitが最良の性能を発揮したと報告した[100]。
GC含量が低く二次構造が安定している(つまり、miRNA ΔG が低い)小さなRNAは、RNA量が少ないサンプルからは抽出中に選択的に失われるとの報告がある[ 92 ]。この対策として1μgのRNAキャリア(Torulla Ambion 酵母 RNA)を添加すると回収率が向上するとの報告がある[101]。
Huらは、培養細胞から抽出されたmiRNAの回収率を高めるために市販の抽出キットを最適な手順に改良し、最終的に、吸着プロセスで65%(v/v)エタノール溶液を使用し、溶出ではpH値8.0のTEバッファーを使用して温度を55℃に上げ、miRNA抽出の条件を最適化した。改良された抽出キットは、最適な抽出条件を使用することで、miRNeasy Mini Kit と比較して内因性miR-21の回収を約6倍促進した[102]。
5.-3)マイクロRNA診断検査における正規化の必要性
miRNA定量において、正規化は極めて重要不可欠な校正処理で、1. 内因性コントロール(リファレンス遺伝子)を用いた正規化、2. 外因性コントロールを用いた正規化 、3. 統計学的手法による正規化(NGSデータ解析など)が用いられる。本稿では紙面の都合上、詳細は割愛させていただき、参考文献とmiRNA測定試薬メーカから公開されている資料を提示する。
・異なるプラットフォーム間でのmiRNA定量における課題と、標準化の重要性について広範に評価[103]
・様々なヒト組織におけるqPCRベースmiRNA発現プロファイリングのためのリファレンス遺伝子を提案し、組織特異的な適切な遺伝子選択の必要性を示す [104]
・RNA-Seqデータ解析における正規化法の選択:RPKM値でサンプル間比較は危険?! [105]
・マイクロRNA測定技術の最近の動向 東レリサーチセンター[106]
・内在性コントロールの選択 | Thermo Fisher Scientific - JP[107]
・最も信頼性の高い正規化方法を正確に選択することの重要性を指摘[108]
6.試料からのmiRNA抽出・精製方法
miRNA測定試料には、PCR阻害因子や、測定を妨げる他の生体分子(タンパク質、脂質など)が含まれるためこれらの夾雑物を除去しないと測定反応が干渉を受ける。また、試料中のmiRNAの量が非常に少なく、測定可能域まで濃縮すべきケースもある。さらに精製することでRNA分解酵素(RNase)の影響を最小限に抑え、サンプルの安定性を高めるなどの効果が得られる。この測定前の一連の処置を抽出・精製操作で行う。
試料からのmiRNA抽出・精製方法は試料の種類(細胞、組織、血清、血漿、その他の体液など)や、その後の解析手法(次世代シーケンシング(NGS)、リアルタイムPCRなど)によって異なる。miRNA抽出・精製 に求められることは、前述の様に試料中の夾雑物を除去しmiRNA(類縁物質を含むncRNA全般)を高収量・高品質の小分子RNAを全回収する事である。現在、一般的な使用傾向としては、有機溶媒抽出法(液相抽出法)もしくは固相抽出法(カラム精製法、磁気ビーズ法)の2つの主要なアプローチが用いられている。近年では、抽出・精製を省略、あるいは簡素化して直接測定する手法も開発されている[109][110]。
6.-1)主要な抽出・精製法
〔6.-1) ~ 7.は, Google AIモードにて複数のキーワードを連立した和文または英文で複数検索し、得た回答を一部PubMed等で検証し、集約後に編集した。〕
A. 有機溶媒抽出法(液相抽出法 例:Trizol 試薬法)
概要:TRIzol(またはそれに類する試薬)を使用したグアニジニウム酸-フェノール抽出法。最も一般的な方法である。
TRIzol試薬法は、細胞や組織から高品質な全RNAを抽出するための方法である。
フェノールとグアニジンイソチオシアネートを含むTRIzol試薬をサンプルに加えて細胞を溶解させ、その後の遠心分離によってRNA、DNA、タンパク質が分離する原理に基づいている。これにより、RNAは上層の水相に、DNAとタンパク質はそれぞれ異なる下相に分かれ、水相のRNAを回収する。
TRIzol試薬法の基本的な手順
- ①細胞/組織の溶解:サンプル(組織または細胞)をTRIzol試薬に加えて均一に溶解・ホモジナイズする。
- ②層分離:クロロホルムを加えて混合し、遠心分離
- ③RNAは上部の水相に移行
- ④DNAとタンパク質は、それぞれ中間相とフェノール相に分離
- ⑤RNAの沈殿と回収:水相を別のチューブに移し、イソプロパノールを加えてRNAを沈殿させる
- ⑥洗浄と精製:RNAペレットをエタノールで洗浄し、乾燥させてから、RNaseフリーの水に再度溶解して精製
- 長所:
- 抽出効率が非常に高く、特にmiRNAの回収率に優れている。幅広い種類の小分子RNAを効率よく単離できる。
- 短所:
- フェノールやクロロホルムなど有害試薬を使用するため、取り扱いに注意が必要。操作工程が煩雑で、熟練を要する場合や、相分離が不完全になるリスクがある。
B. 固相抽出法(カラム精製法、磁気ビーズ法 例:シリカゲルメンブレンベースのキット)
TRIzol法と組み合わせて、または完全にフェノールフリーの方法として、多くの市販キットが用いられている。
概要:溶解した試料をシリカカラムに通し、特定の結合条件(エタノール濃度など)を利用してRNAを結合・洗浄・溶出させる方法
シリカメンブレンカラムや磁気ビーズを用いた市販の抽出キット(例:QIAGENのmiRNeasyキット、PromegaのReliaPrep™ miRNAシステムなど)がある。
miRNAを含むトータルRNAを抽出できるキット(例:QIAGENのmiRNeasyシリーズ、Thermo Fisher ScientificのmiRvanaシリーズ、Norgen Biotekの製品など)が特に頻用されている。これらのキットは、小分子RNAの結合効率を高める工夫がされている。
- 長所:
- 操作が簡便で、有害試薬の使用が抑えられる。自動化しやすく、サンプル間の一貫性・再現性が高い傾向がある。
- 短所:
- 収量が有機溶媒抽出法に比べて劣ることがある。特に血清や血漿などRNA量が極めて少ないサンプルでは、キャリアRNAの添加などが推奨される。
C. 磁気ビーズ法
自動化に適しており、ハイスループットな実験系で利用される
収量はカラム法より低い場合があるが、簡便さが利点である。
推奨されるアプローチ
高い収量と純度を求める場合:丁寧に実施すれば、TRIzol法などの有機溶媒抽出法が高い評価を得易い。
簡便さ、再現性、安全性を求める場合:各種の市販キットが優れている。特に、体液などからの抽出用に設計された専用キットが各社から市販されている。
市販のmiRNA専用カラム精製キット(例:QIAGENのmiRNeasyシリーズ、PromegaのReliaPrep™ miRNA kit)が広く利用され、高い評価を得ている。
これらのキットは、通常、化学的溶解ステップとそれに続くカラム精製ステップを組み合わせている
重要なポイント
血清・血漿などの体液試料:体液はmiRNAの絶対量が非常に少ないため、専用のキット(例:miRNeasy Serum/Plasma Advanced Kit)の使用が推奨される。これらのキットでは、抽出効率を評価するために外因性のスパイクインコントロール(合成miRNAなど)を追加することが重要である。
抽出後のmiRNAの品質と量を、分光光度計やキャピラリー電気泳動(Bioanalyzerなど)で評価することが大切である。
抽出・精製法は、実験目的、予算、扱える試料量、および研究室の設備や習熟度を考慮して、最適な方法を選択する。また、抽出・精製に関する最新の情報収取にも努める。
6.-2)抽出・精製に関する文献例
以下に、抽出・精製方法の比較評価や特定のキットの有効性を示した文献を示した
112) Brown RAM, et al. BMC Biotechnol. 2018 Mar 16;18(1):16.
この研究では、マウスの肺、肝臓、脳組織から5種類の市販トータルRNA抽出キット(TRIzol、miRvana、miRNeasy、Norgen製品など)を用いてRNAを抽出し、品質、収量、miRNA発現解析への適合性を比較。
結論として、フェノール・クロロホルム相分離とそれに続くシリカカラム抽出を組み合わせた手法(miRvana microRNA isolation kitなど)が、一貫した品質と高いmiRNA回収率をもたらす点で優れていたと報告[93]。
血漿からのmiRNA抽出において、TRIzol処理後にグリコーゲンを共沈剤として使用し、QIAGEN miRNeasy Mini Kitで精製する方法が、内因性miRNAの最も高い回収率をもたらした[111]。
Trizol試薬を用いて全RNAを分離し、巨大RNAを沈殿後に、酢酸カリウムを添加し、終濃度2.5 M LiClとエタノールを用いて小分子RNAを沈殿させることで、ほとんどの臨床検体に応用可能な高収量・高品質の小分子RNAを得た[112]。
これらの文献は、特定の試料(組織や血液)に対してどの手法が最適かを比較検討しており、実験目的に応じた適切な方法の選択が重要であることを示唆している。多くの研究において、再現性と簡便さから市販の専用キットが選択される傾向にある。
血漿マイクロRNA抽出のための改良プロトコルの評価[113]。
miRNA シーケンスのための細胞外小胞分離方法の比較[114]。
7.マイクロRNA測定法
A. 定量リアルタイムPCR(RT-qPCR)法
miRNAの定量リアルタイムPCR(RT-qPCR)法は、極めて短い配列のmiRNAを、高い特異性と高感度で定量するための特殊な技術・工夫が必要である。
ここでは、代表的な方法である「ステムループRT-qPCR法(TaqMan法)」と「ポリA付加RT-qPCR法(SYBR Green法)」を中心に解説する。
なぜmiRNAの定量は難しいか?
mRNAのRT-qPCRが比較的容易なのに対し、miRNAの定量には以下のような課題がある。
配列の短さ:成熟miRNAは一般的に約18-25塩基と非常に短いため、標準的なプライマー設計が難しい。
少量の存在量:多くのmiRNAは細胞内で低レベルでしか発現しておらず、感度の高い検出が必要となる。
高い相同性:互いに非常に似た配列を持つmiRNAファミリーメンバーが多く、高い特異性で区別する必要がある。
miRNA定量RT-qPCRの基本ワークフロー
miRNAの定量RT-qPCRは、大きく以下の2つのステップで構成されます。
ⅰ逆転写(Reverse Transcription:RT):サンプルから、miRNAを鋳型として相補的DNA(cDNA)を合成する。
ⅱリアルタイムPCR: cDNAを増幅しながら蛍光を検出し、そのサイクル数(Ct値)から元のmiRNA量を定量する。
主なmiRNA定量RT-qPCRの方法
(A-ⅰ)ステムループRT-qPCR法(TaqMan法)
サーモフィッシャーサイエンティフィック社の「TaqMan MicroRNA Assays」に代表される方法。
特徴
高い特異性:ステムループ構造を持つmiRNA特異的なプライマーを用いることで、成熟miRNAのみを選択的に認識・増幅できる。
高い感度と再現性:少量のサンプルでも正確に定量でき、再現性にも優れている。
広いダイナミックレンジ:微量から多量まで、幅広い発現量のmiRNAを定量できる。
原理
- ①ステムループプライマーによる逆転写:miRNAの3'末端に特異的に結合するステムループ構造の逆転写プライマーを用いて、miRNAからcDNAを合成する。
- ②リアルタイムPCR:合成されたcDNAを鋳型として、miRNA特異的なフォワードプライマーと、ステムループ配列に対応するユニバーサルリバースプライマーを用いてPCRを行う。
- ③TaqManプローブによる検出:増幅の進行に伴って、蛍光標識されたTaqManプローブが分解され、蛍光が放出される。この蛍光強度をリアルタイムで測定する。
(A-ⅱ)ポリA付加RT-qPCR法(SYBR Green法)
miRNAにポリA配列を付加する工程を含む方法である。
特徴
柔軟なプライマー設計:ポリA付加とユニバーサルなオリゴdTプライマーを用いることで、複数のmiRNAを一度に逆転写することが可能である。
SYBR Greenによる検出:比較的安価なSYBR Green蛍光色素を用いることができる。
非特異的増幅のリスク:プローブを使用しないため、SYBR Greenは非特異的に生成された二本鎖DNAにも結合し、偽陽性の原因になる可能性がある。これを防ぐため、融解曲線解析で増幅産物の特異性を確認する。
原理
- (1)ポリA付加:miRNAの3'末端に、ポリAポリメラーゼを用いてポリA配列を付加する。
- (2)オリゴdTプライマーによる逆転写:ポリA配列に相補的な配列と、それに続いてユニバーサルな配列を持つオリゴdTプライマーを用いてcDNAを合成する。
- (3)リアルタイムPCR:合成されたcDNAを鋳型として、miRNA特異的なフォワードプライマーとユニバーサルなリバースプライマーを用いてPCRを実施する。
- (4)SYBR Greenによる検出:PCR産物の二本鎖DNAにSYBR Greenが結合することで蛍光を発し、増幅をモニタリングする。
表1に ステムループRT-qPCR法(TaqMan法)とポリA付加RT-qPCR法(SYBR Green法)の利点と欠点を一覧化した。
表1ステムループRT-qPCR法(TaqMan法)、ポリA付加RT-qPCR法(SYBR Green法)の利点と欠点
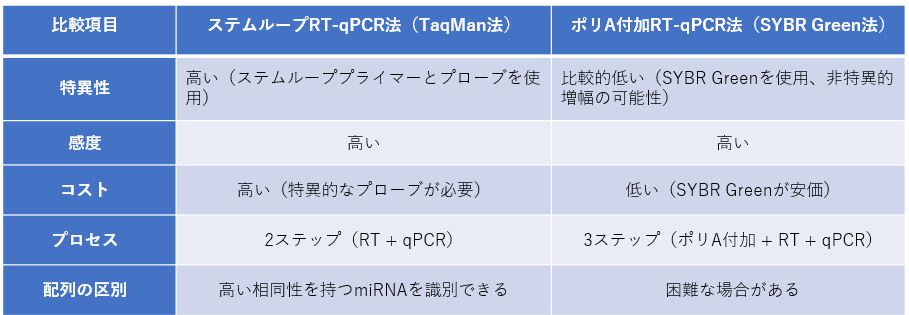
(Google AIモードより引用)
研究目的、必要な特異性、予算などに応じて適切な方法を選択することが重要です。
B. マイクロアレイ法
miRNAマイクロアレイ法は、スライドガラス基板上に合成された数千種類ものmiRNAプローブ(短いDNA断片)を用いて、特定の細胞や組織に含まれるmiRNAの発現パターンを網羅的に解析する技術です。遺伝子発現の調節に関わるmiRNAの変化を一度に大量に測定できる。
原理
miRNAマイクロアレイ法は、核酸のハイブリダイゼーションを応用している。
- ①RNAの抽出:まず、解析対象となる細胞や組織から、すべてのRNAを抽出。この際、小さなmiRNAが失われないように注意が必要である。
- ②標識:抽出したRNAサンプル中のmiRNAを、蛍光色素で標識する。比較実験の場合、異なるサンプル(例:健常群と疾患群)由来のmiRNAをそれぞれ異なる色の蛍光色素(例:Cy3とCy5)で標識する。
- ③ハイブリダイゼーション:標識したmiRNAを、基板上のmiRNAプローブに結合させる。miRNAと相補的な配列を持つプローブがあれば、miRNAが結合(ハイブリダイゼーション)する。
- ④洗浄とスキャン:ハイブリダイゼーション後、結合しなかったmiRNAを洗い流し、スキャナーで蛍光強度を測定する。蛍光の強度は、サンプル中に含まれる特定のmiRNAの量に対応する。
- ⑤データ解析:異なるサンプルで得られた蛍光強度を比較することで、発現量に差のあるmiRNAを特定する。これにより、特定の疾患や条件下でmiRNAの発現がどのように変動しているかを分析できる。
利点
網羅的解析:大量のmiRNAを同時に測定できるため、miRNAの発現パターン全体を一度に把握できる。
迅速性:次世代シーケンサー(NGS)に比べて、比較的短期間で解析結果が得られる。
簡便性:実験ワークフローが確立されており、NGSに比べてサンプル調製やデータ解析が比較的容易である。
相対的定量:複数のサンプル間でmiRNAの相対的な発現量を比較するのに適している。
欠点
既知のmiRNAのみ対象:基板上のプローブに合うmiRNAしか検出できないため、未知のmiRNAや新規変異の検出はできない。
絶対定量の難しさ:NGSのような絶対的な定量は難しく、相対的な発現量の比較が主になる。
多くのRNA量が必要:NGSと比較すると、より多くのRNA量が必要になる場合がある。
高い特異性:配列のわずかな違いを区別しにくい場合があるため、得られた結果を別の手法(例:qRT-PCR)で検証することが推奨される。
応用例
miRNAマイクロアレイ法は、miRNAの関与するさまざまな生命現象や疾患研究に応用されている。
疾患のバイオマーカー探索:健常者と疾患患者(がん、心血管疾患、神経疾患など)の組織や体液中のmiRNA発現パターンを比較することで、診断や予後予測に役立つバイオマーカーを特定する。
薬物スクリーニング:候補薬物がmiRNAの発現に与える影響を評価し、作用機序の解明や新規治療薬の開発に利用される。
細胞分化・発生メカニズムの解明:細胞が分化していく過程でのmiRNAの発現変動を追跡し、細胞の増殖や分化を制御するメカニズムを解明する。
組織特異的発現の解析:組織ごとに異なるmiRNAの発現パターンを調べることで、miRNAの組織特異的な役割を明らかにする。
表2に miRNA解析におけるマイクロアレイ法と次世代シーケンサー(NGS)との比較を示した。
表2 miRNA解析におけるマイクロアレイ法と次世代シーケンサー(NGS)との比較
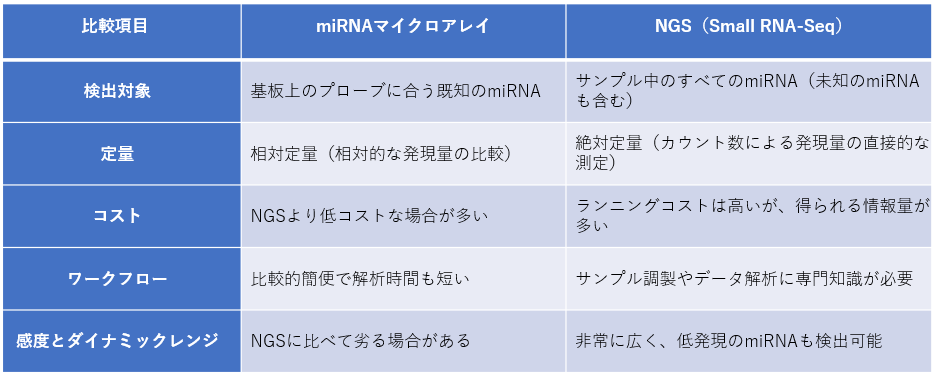
(Google AIモードより引用)
近年、NGS技術の普及により、miRNA解析の中心はマイクロアレイからNGSへと移行しつつあります。
マイクロアレイは、既知のmiRNA発現パターンを迅速かつ手軽に比較したい場合に有用であるが、新規miRNAの発見やより精密な定量が必要な研究では、NGSが選択されることが多くなっている。
C. 次世代シーケンサー(NGS)法
miRNAの次世代シーケンサー(NGS)法(miRNA-seq)は、特定の生物学的サンプル中に存在する既知および新規miRNAの配列と発現量を網羅的に解析する技術です。疾患のバイオマーカー探索や、miRNAによる遺伝子発現制御機構の解明に広く利用されている。miRNAは非常に小さな非コードRNAなため、特殊なプロトコルとデータ解析方法が用いられる
実験の主な流れ
miRNA-seqのワークフローは、主に「サンプル調製」「ライブラリー調製」「シーケンシング」「データ解析」の4つの段階に分かれる。
- ① サンプル調製
高品質RNAの抽出:最初のステップは、組織、細胞、体液など、目的のサンプルから質の良い全RNAを抽出する。RNAの分解を防ぎ、miRNAを含む「small RNA」を確実に回収することが重要である。
小分子RNAの確保:は非常に短いため、抽出過程で分解されないよう細心の注意が必要で、組織、血清、血漿、エクソソームなど、多様なサンプルにも対応した抽出法である。 - ② ライブラリー調製
ライブラリー調製は、NGS解析の成否を左右する重要なステップである。miRNA(約22ヌクレオチド)をNGSプラットフォームで読み取れるようにするため、miRNAの3‘末端と5’末端にアダプターを付加してシーケンスライブラリーを作製する。
- ⅰ.アダプターの付加:は短いため、シーケンスの足がかりとなるアダプターと呼ばれるオリゴヌクレオチドを両端に付加する。
・3'アダプターは、特定のRNAリガーゼを用いてmiRNAに特異的に結合させる。
・その後に5'アダプターを結合させる。 - ⅱ.逆転写(cDNA合成):アダプターが付加されたmiRNAを鋳型として、逆転写酵素によりcDNAを合成する。
- ⅲ.PCR増幅:合成されたcDNAをPCRで増幅し、シーケンスに必要な量のDNAライブラリーを準備する。(シーケンス用のライブラリーを構築 する。)
- ⅳ.アダプターダイマーの除去:ライブラリー調製の過程で生じるアダプター同士が結合した不純物(アダプターダイマー)を、サイズ選択などによって除去します。
- ⅰ.アダプターの付加:は短いため、シーケンスの足がかりとなるアダプターと呼ばれるオリゴヌクレオチドを両端に付加する。
- ③ シーケンシング
ライブラリー調製後、NGSプラットフォーム(例:Illumina社の機器)を用いて、ハイスループットなシーケンシングを行います。この工程で、膨大な数のmiRNA配列データ(リード)が生成する。
- • NGSプラットフォーム:などのNGSプラットフォームを用いて、調製したライブラリーを大量に並列処理で読み取る。
- • ショートリード:miRNAは短いため、短鎖の配列(ショートリード)が大量に生成される。
- ④ データ解析
膨大なリードを解析し、miRNAを同定、定量する。miRNA-seqデータの解析には、専用のバイオインフォマティクスパイプラインが必要である。
- • リードの前処理:span>シーケンスデータの品質チェックを行い、ライブラリー調製時に付加したアダプター配列や低品質の配列を除去する。
- • マッピングと定量:処理されたリードを、miRNAのデータベース(miRBaseなど)やリファレンスゲノムにマッピングし、既知のmiRNAを同定する。各miRNAの発現量をカウントし、正規化後定量する。
- • 新規miRNAの予測:既知miRNAデータベースにマッピングされないリードから、新規miRNAを予測・同定する。
- • 発現変動解析:異なるサンプル間(例:疾患群と健常群)で、miRNAの発現量に有意な差があるかを統計的に解析し、発現が変動しているmiRNAを特定する。
- • 可視化と機能解析:統計結果をヒートマップやボルケーノプロットなどで可視化し、miRNAの標的遺伝子予測やパスウェイ解析、生物学的プロセスを解析する。
主な利点と応用
網羅的な解析:サンプル中の既知miRNAの発現プロファイルだけでなく、新規miRNAの同定も可能である。
高感度・高精度:微量なmiRNAでも高感度で検出でき、発現量を正確に定量できる。
バイオマーカー探索:既知のmiRNAだけでなく未知のmiRNAやアイソフォーム(isomiR)まで検出できる高い網羅性と感度が利点で、この特性を生かし、さまざまな疾患のバイオマーカー探索に応用されている。
新規治療標的の同定:miRNAの発現制御メカニズムを解明することで、新たな創薬標的を見つけることもできる。
表3にmiRNAのNGS法、定量PCR(qRT-PCR)法およびマイクロアレイ法と3法の特性を一覧化した。
表3 miRNAのNGS法、定量PCR(qRT-PCR)法およびマイクロアレイ法の特性の比較
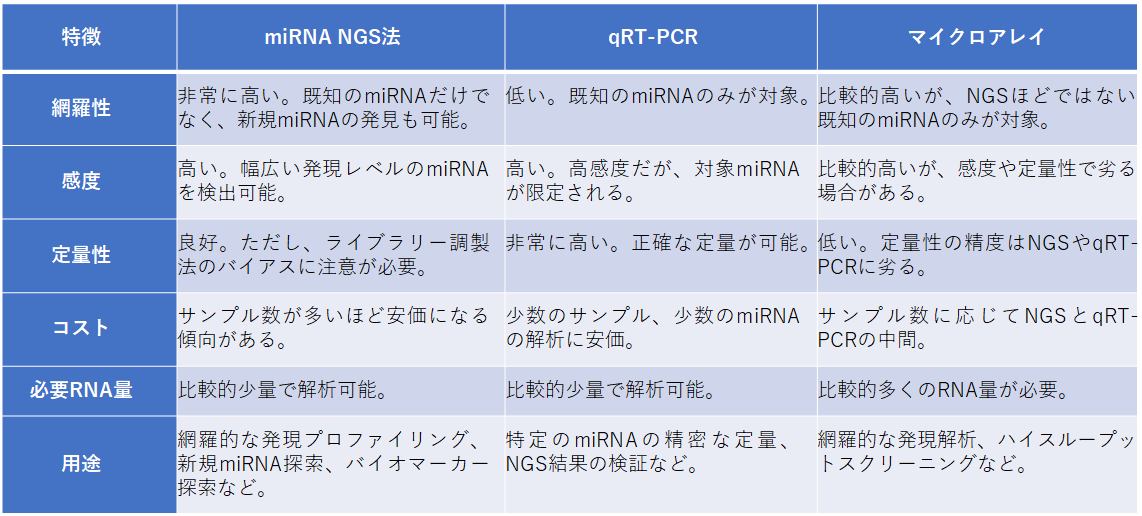
(Google AIモードより引用)
D. LNA(Locked Nucleic Acid)プローブ法[115]
マイクロRNA分析におけるLNA(Locked Nucleic Acid:LNAまたは架橋型核酸(Bridged Nucleic Acid:BNA)プローブ法は、LNAという特殊なゼノ核酸(ゼノ核酸(xeno nucleic acids: XNA)は、天然の核酸であるDNAやRNAとは異なる糖骨格をもつ合成核酸アナログである)を導入することで、標的であるマイクロRNA(miRNA)への結合親和性と特異性を飛躍的に高めた分析手法が開発された。特に、ごく短いmiRNAの検出において、従来のプローブでは困難であった感度と特異性の課題に飛躍的な成果が見られる。
LNAプローブ法の原理
1)LNAの化学構造:LNAは図1に示した様に、リボース環の2位の酸素原子と4位の炭素原子がメチレン基で架橋された環状構造を持つ人工核酸です。
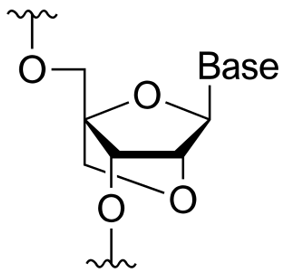
図1 LNAの構造
2)高い結合親和性:は、独特の環状構造によって構造の自由度が少なく、架橋構造によってリボース環の立体構造が固定され、DNAやRNAの相補鎖に対して非常に強固なハイブリダイゼーション(結合)が可能になる。
3)融解温度(Tm値)の上昇:LANを含むオリゴヌクレオチドは、プローブと標的miRNAとのハイブリッドの融解温度(Tm値)が大幅に上昇する。Tm値が高いほど、より厳密な条件下(高温、低塩濃度)でも安定して結合するため、非特異的な結合を排除できる。
4)高い特異性:LNAは、塩基配列のミスマッチを厳密に区別する能力が非常に高く、わずか1塩基の違いも識別できる。この特徴は、塩基配列が非常に似ている複数のmiRNAのファミリーを区別する上で重要である。
5)miRNAの検出:LNAプローブは、この特性を利用して、配列長が短く、通常のプローブでは検出が困難であったmiRNAを、高い特異性で検出できる。
LNAプローブを用いた主な分析法
現在では、LNAプローブは、さまざまなマイクロRNA分析法に応用されている。
〇 リアルタイムPCR(qPCR)
- ・LNAを組み込んだプライマーやプローブを用いることで、miRNAの正確な定量が可能になる。
- ・逆転写反応とPCRを組み合わせることで、微量なmiRNAでも高感度に検出できる。
〇 ノーザンブロッティング
- ・従来の核酸プローブよりも感度と特異性が高いため、微量なmiRNAの検出がより正確に行える。
〇 in situハイブリダイゼーション(FISH)
- ・細胞や組織内のmiRNAを可視化する際に使用され、LNAの特異性の高さにより、微小なmiRNAを高感度に検出できる。
〇 マイクロアレイ解析
- ・マイクロアレイ上の捕捉分子にLNAを組み込むことで、多数のmiRNAを網羅的に解析でき、かつ、Tm値が均一化されるため、最適なハイブリダイゼーション条件で親和性を高め、検出感度を高めることができる。
メリット
高感度:短い配列のmiRNAでも、高い結合親和性によって効率的に捕捉できるため、微量なmiRNAの検出が可能。
高特異性:1塩基のミスマッチでも厳密に識別できるため、miRNAファミリー間の類似配列を区別できる。
高い熱安定性:融解温度(Tm)が高いため、熱変性に強く、安定した実験が可能。
デメリット
コスト:LNAは特殊な化学修飾核酸であるため、通常のDNAやRNAプローブに比べて製造コストが高い。
プローブ設計の複雑さ:優れたプローブを設計するには、LNAの組み込み位置や数などを慎重に検討する必要があり、専門的な知識が求められる。
8.マイクロRNA診断:測定技術の進化
消化器癌における成熟マイクロRNAの異なるメチル化レベル
『マイクロ(mi)RNAの生物学的意義は、従来、miRNAが標的を不変的に認識・制御するという仮定に基づき、RNA発現レベルに基づいて評価されてきた。本研究では、miR-17-5p、-21-5p、-200c-3p、let-7a-5pなどの成熟miRNAの一部が、その安定性と標的認識を変化させる可能性のあるメチル化マークを有することを示す。重要な点として、これらのmiRNAのメチル化は、対照群の正常組織と比較して、がん組織で有意に増加していた。さらに、血清検体中のmiR-17-5pメチル化レベルは、早期膵臓がん患者と健常対照群を極めて高い感度と特異度で区別することができた。これらの知見は、早期がんの診断戦略の基礎となり、miRNA生物学の理解に新たな次元を加えるものである。
Nat Commun. 2019 Aug 29;10(1):3888. Abstractを和訳引用 [116]』
1. 新技術・測定方法
〇 デジタルPCR(dPCR):
- ● 従来のリアルタイムPCR (qPCR) よりも高感度なmiRNA定量技術として普及が進んでいる。特に微量サンプルや、発現量が非常に少ないmiRNAの検出に強みがある。
- ● QIAGENなどの企業からデジタルPCR用のmiRNAアッセイキット(例: miRCURY LNA miRNA PCR Assays)が提供されている。
〇 次世代シーケンシング (NGS) を利用した網羅的解析:
- ● 多数のmiRNAを一度に、網羅的に解析する手法として引き続き重要です。東レの「3D-Gene®」マイクロアレイシステムなども、信頼性の高い網羅的解析プラットフォームとして活用されている。
〇 ナノポアシーケンシング:
- ● ナノポア(極小の穴)をmiRNAが一分子ずつ通過する際の電気信号を検出することで、miRNAを一分子レベルで直接、迅速に診断・検出する技術が研究されている。
〇 「RNA液滴コンピュータ」:
- ● 複数の特定miRNAを選択的に同時に認識し、その組み合わせに応じた結果を出力できる新しい検出システムが開発された(理化学研究所、京都大学などによる共同研究)。がんのバイオマーカー検出などへの応用が期待される[117]。
〇 細胞内miRNA濃度定量技術:
- ● 細胞内のmiRNAの分布や局所濃度を簡便かつ高精度に可視化・定量できる新技術が開発された。独自の「二足歩行型DNAウォーカー」設計などを利用し、細胞環境の影響を補正して検出する。(北海道大学)[118]
2. 新しい試薬・機器
〇 自動核酸抽出装置と専用試薬:
- ● 血清、血漿、FFPE標本(ホルマリン固定パラフィン包埋標本)など多様なサンプルからmiRNAを含むトータルRNAを効率的に抽出するための自動化装置と専用試薬が開発されている(例: プレシジョン・システム・サイエンスの「magLEADシリーズ」と「MagDEA Dx SV miRNA」試薬キット)。
〇 エクソソームからのmiRNA抽出キット:
- ● エクソソーム(細胞外小胞)内のmiRNAは新しいバイオマーカーとして注目されており、エクソソームからmiRNAを効率よく抽出・検出するための専用試薬キットが市場に登場している(東洋紡など)。
〇 ハイスループットな分析機器:
- ● 一度に多数のサンプルを処理できる機器が求められており、96サンプルプレートに対応したデジタルPCRシステム(ユーロフィンなど)が利用可能である。
〇 エピタコフォレシス(Epitachophoresis)は、臨床的に重要なサンプルから DNA と RNA を同時に分離できる新しい次世代抽出システムです。長さ(20 nt~290 Kbp)にわたる多様な核酸を抽出することで、エピタコフォレシスの汎用性を高めている。抽出された miRNA、mRNA、gDNA の品質は、下流の次世代シーケンシングによって評価された。エピタキオフォレシス(ETP)は、先導電解質と後続電解質からなる不連続電解質システムを利用して、核酸を狭いバンドに集中させる。ETP システムでは、アガロースゲルが電解質溶液を安定化させ、核酸のサイズ選択アプリケーションを可能にする。適用可能な場合、ゲルを非ふるいマトリックスに置き換えて、大きな DNA フラグメントを濃縮することもできる。ETP は、サンプルが外側のリングにロードされ、中央のウェルから液体抽出物としてピペットで排出される独自の円形アーキテクチャを利用している[119]。
9.miRNAを含むncRNA今後の展望
分子生物学的理念からの個別化医療は、その意識浸透に始まり、期を同じくして、バイオインフォマティクス、シーケンシング、プロテオミクス、マイクロアレイ、機械学習、AI等の概念の普及および分析機器や革新技術の導入に伴い急速な進展を遂げている。結果として、miRNA、lncRNA、circRNAなどの多種多様な非コード RNA (ncRNA) が特定され、その機能解明も進展している。これらは、主に真核生物の複雑さに関連するほとんどの細胞メカニズム調節因子を構成しており、疾患発症、疾患進展機構への関与が解明され、さらには診断バイオマーカー・治療薬としての活用が研究されている。この様な状況において、特にmiRNAの研究は活況でありその成果も多くの疾患について研究されている。miRNAは、生物学的機構の複雑性としては、SNPs、IsomiRの存在、競合的内因性RNA(ceRNA)、1つのmiRNAは複数のmRNAを制御するなどの構造機能的特性を有するためにいっそう難解さを増している。さらに今後は、NGS技術を用いた次世代RNAシーケシング(RNA-seq)技術が普及しており、さらなるncRNA分野全体の分子機能解明と構造解析情報が増すものと思われる。これに伴い、miRNAパネルが多様化しAI・機械学習等とののコンビネーションが進化・進展し広範囲の疾患診断の予兆のみに終わらず健康変調管理すらも可能となるかも知れない。
これら基礎研究の進展を機にncRNA分子の卓越した高い有益性の発見の蹶起に押され、ncRNA分子の疾患診断応用への課題が改善され、診断検査として活況を期すことを望みたい。
疾患においては、がんにおいて重要視される早期診断は、いずれの疾患においても云える。患者の寛解率と全生存率の向上を目指し、増大する疾患の負担を軽減する取り組みにおいて極めて重要である。しかし、この差し迫った必要性にもかかわらず、多くの腫瘍の無症状の性質、併存疾患、感度と特異度の高いスクリーニング検査の欠如など、目に見えないがんを考えると、無数の課題が存在する。この様な状況下、前述のmiRNA は、有望な早期診断がんバイオマーカーと云える(これは他の疾患でも同様である)。NSCLCやHCCなどの鑑別が難しいさまざまながんに対する診断の感度と特異度の高いmiRNAシグネチャーが文献で十分に報告されているほか、多くの膵炎患者と膵臓がん患者を正確に識別できる。診断分野は、miRNAの検出強化が報告されるなど、進展し続けている。 Nanostringの nCounter® microRNAアッセイや次世代RNAシーケンシング(RNAseq)などの市販プラットフォームは、感度と特異性の点でかつてゴールド スタンダードと考えられていた RT-qPCRを上回っており、他の新しいセンシング技術はさらに高い感度とLOD率、および強化されたマルチプレックス機能を提供している。さらに、進化的教師ありAI学習法 CancerSigなどのバイオインフォマティクスと機械学習の統合により、スケーラブルで再現可能な自動化された手段による予測モデリングを介して、有望なmiRNAシグネチャーをさらに特定できる。しかし、がんバイオマーカーとしてのmiRNAの期待にもかかわらず、臨床応用を考えると幾つもの課題が存在する。これらの課題の多くは、本質的には固有のものですが、科学コミュニティ内での団結した協力的な取り組み、オープンソース プラットフォームを介したデータセットの共有、標準化されたプロトコルの適用、自動化および技術の進歩などの協調によって到達可能となる。もう少しで手が届きそうなところまで近づいている気配が伺える。
おわりに
従来は、診断のバイオマーカーはタンパク質本位の理念であったがそのタンパク質発現を制御する機能を持つmiRNAは、疾患発症の初期対応から関与する重要な分子である。したがって疾患初動時の代謝に呼応する発症初期の無症状期においてすらも検知できる可能性を有する感度と特異度の高いスクリーニング検査となりうる可能性を秘めている。さらに診断においても膵炎と膵がん等の様に、これまで生体反応においては全く異質の代謝病状ながら困難であった鑑別診断ができる。また、一部の疾患の患者においては、転帰の予後・予測が推察可能となり治療選択ができる。さらに、これまでは、症状の発症は認められても、もしくは自覚症状は有っても診断がつかず病院巡りや時間を浪費した患者の苦悩が軽減されるかも知れない。また、健康を自負する方の突然死の何割かは未然に防げるかも知れない。また、病態の研究を深めることにより進行ステージが判明し同じ疾患でも治療内容が変更されるかも知れません。感染症からアレルギー発症の疾患移行期の変遷期の判明に伴う治療変更。miRNAのパネル化による診断領域の拡張などなど、miRNAを含むncRNAの医療への応用によっては医療体系の変革が求められるかも知れない。
『1種類のmiRNAは複数のmRNAを制御することができ、1種類のmRNAは複数のmiRNAによって制御されている。』これまで、ヒトの頭脳に依存してきた診断学に機械学習・AIの支援は不可欠となり、これまでは研究分野のみでの活用で有った分子生物学的手法が臨床検査技術として導入される日も遠くないかも知れない。
参考文献・資料
- Mussbacher M, et al. Cells. 2020 Aug 18;9(8):1915.
- Grimaldi AM et al., Biomedicines. 2022 Oct 31;10(11):2766.
- Sun G, et al. RNA. 2009 Sep;15(9):1640-51.
- Tomasello L, et al. Front Cell Dev Biol. 2021 Jun 9;9:668648.
- Salmena L, et al. Cell. 2011 Aug 5;146(3):353-8.
- Yang N, et al. J Oncol. 2021 Oct 7; 2021:4279039.
- Bartel DP. Cell. 2004 Jan 23;116(2):281-97.
- Asano N, et al. Nat Commun. 2019 Mar 21;10(1):1299.
- Tan HM, et al. Int J Mol Sci. 2022 Jul 15;23(14):7804.
- Liu, S. et al. Sci Rep 7, 15328 (2017).
- Mihai AM, et al. J Med Life. 2024 Jun;17(6):549-554.
- Jelski, W.et al. Int. J. Mol. Sci. 2025, 26, 4395.
- Baba S, et al. EClinicalMedicine. 2024 Nov 12; 78:102936.
- Ghafouri-Fard S, et al. (2021) Front. Cardiovasc. Med. 8:632392.
- Lin J, et al. Open Med. (2019) 15:1–7.
- Lin Y, et al. Kidney Blood Pressure Res. (2020) 45:477–96.
- Liu Y, et al. Circul Res. (2019) 124:575–87.
- Hou S, et al. Biochem Biophys Res Commun. (2017) 484:27–33.
- Wang M, et al. Med Sci Monit. (2016) 22:5011.
- Su Y, et al. Cell Death Dis. (2019) 10:1–15.
- Yang S, et al. J Cell Mol Med. (2018) 22:2739–49.
- Lian Z, et al. J Cell Biochem. (2018) 119:6684–94.
- Bai F, et al. Aging. (2019) 11:3198.
- Vahed SZ, et al. Gene. (2019) 698:170–8.
- Lai Z, et al. Biomed Pharmacotherap. (2018) 97:162–7.
- Witarto BS, et al. Diabetes Metab Syndr. 2023 Oct;17(10):102860.
- Han X, et al. BMC Cardiovasc Disord. 2021 Mar 24;21(1):150.
- Michael T McManus, Seminars in Cancer Biology, Volume 13, Issue 4, August 2003, Pages 253–258.
- Wisløff U, et al. Science. 2005 Jan 21;307(5708):418-20.
- Chisato Kinoshita, et al. Nature Communications 5, Article number: 3823.
- Carrie Wright, et al. Front Genet. 2013; 4: 58.
- Jenny Buckland. Nature Reviews Rheumatology 6, 436 (August 2010).
- Qinghua Jiang, et al. Nucl. Acids Res. (2009) 37 (suppl 1): D98-D104.
- Bert Vogelstein, et al. Science 29 March 2013: Vol. 339 no. 6127 pp. 1546-1558 .
- George Adrian Calin, et al. PNAS March 2, 2004 vol. 101 no. 9 2999–3004.
- Jun Lu, et al. Nature 435, 834–838 (9 June 2005).
- Leslie K. Ferrarelli,Sci. Signal. 8, eg3 (2015).
- Calin GA, et al. Proc Natl Acad Sci U S A. 2002 Nov 26;99(24):15524-9. Epub 2002 Nov 14.
- Massimo Negrini, et al. J Cell Sci. 2007 Jun 1;120(Pt 11):1833-40.
- George A. Calin & Carlo M. Croce、Nature Reviews Cancer 6, 857-866 (November 2006) .
- Jason F. et al., Cancer Res July 15, 2010 70; 5923.
- Baohong Zhang, et al. Developmental Biology. Volume 302, Issue 1, 1 February 2007, Pages 1–12.
- O A Kent and J T Mendell. Oncogene (2006) 25, 6188–6196.
- Fanyin Meng, et al. Gastroenterology, August 2007, Volume 133, Issue 2, Pages 647–658.
- Iorio MV, et al. Cancer Res 2005;65:7065–70.
- Xu J, et al. Oncol Rep. 2015 Jun;33(6):3108-16.
- Masahiro Seikea, et al. PNAS July 21, 2009 vol. 106 , no. 29 , 12085–12090.
- Chung Wah Wu, Simon S M Ng, et al. Gut 2012;61:739-745.
- Cheng CY, et al. Cell Rep. 2014 Mar 27;6(6):1000-7.
- Shi Y, et al. PLOS One. 2014 Mar 4;9(3): e90022.
- Gao J, et al. Oncogene. 2015 Jul 30;34(31):4142-52.
- Gougelet A, et al. Gut. 2015 Mar 19. pii: gutjnl-2014-308969.
- Pedro P. Medina, Mona Nolde & Frank J. Slack Nature 467, 86–90 (2010)
- Garzon R, et al. Nature Reviews Drug Discovery 9, 775–789 (1 October 2010)
- Morten Lindow et al. J Cell Biol. (2012) Vol. 199 No. 3 407–412.
- Harry L.A. et al. N Engl J Med 2013; 368:1685-1694May 2, 2013.
- R. Persson, et al. EASL - The International Liver Congress 2015 50th annual Meeting of the European association for the Study of the Liver Vienna, austria april 22-26.
- Aaron Bouchie, Nature Biotechnology 31, 577 (2013)
- Kaladhar B Reddy. Cancer Cell International 2015.
- Charles H. et al. Br J Haematol. (2008) May;141(5):672-5.
- Patrick S. et al. PNAS July 29, (2008) vol. 105 no. 30 10513–10518.
- Johan Skog, et al. Nature Cell Biology 10, 1470 - 1476 (2008).
- Josie Hayes, et al. Trends in Molecular Medicine, August 2014, Vol. 20, No. 8。
- Čugura T, et al. Cancers (Basel). 2025 Sep 25;17(19):3123.
- Patel V, et al. Curr Opin Nephrol Hypertens. 2012 Jul;21(4):410-6.
- Zhang X, et al. Yi Chuan. 2025 Jul 20;47(7):729-741.
- Antoun C, et al. Int J Mol Sci. 2025 Feb 28;26(5):2191.
- Jaksic Karisik, et al. Cells 2025, 14, 91.
- Samidurai A, et al. Rev Cardiovasc Med. 2025 May 27;26(5):27966.
- Agahi M, et al. Anal Biochem. 2022 Aug 15; 651:114697.
- Valadi H, et al. Nat Cell Biol. 2007 Jun;9(6):654-9.
- Walter BA, et al. J Cancer. 2013 May 9;4(5):350-7.
- Wang M, et al. Biomed Res Int. 2020 Jul 21;2020:8504238.
- Liu J, et al. Oncotarget. 2017 Mar 21;8(12):20122-20132.
- Zhao J, et al. Front Cell Neurosci. 2021 Nov 2; 15:771898.
- Colaianni F, et al. Genes (Basel). 2024 Oct 12;15(10):1313.
- Singh S, et al. Clin Chim Acta. 2025 Sep 29; 579:120633.
- Matsuzaki J, et al. JNCI Cancer Spectr. 2023 Jan 3;7(1):pkac080.
- Ng L, et al. Int J Cancer. 2025 Feb 15;156(4):865-874.
- Jin X, Clin Cancer Res. 2017 Sep 1;23(17):5311-5319.
- Ji J, et al. J Cancer. 2018 Sep 8;9(19):3435-3446.
- Chen S, et al. Front Genet. 2024 May 16; 15:1371441.
- Li M, et al. Cancer Med. 2019 Nov;8(16):7006-7017.
- Vavassori C, et al. Eur Cardiol. 2022 Mar 7;17:e06.
- Gargiulo P, et al. ESC Heart Fail. 2023 Apr;10(2):753-761.
- Al-Temaimi R, et al. Exp Mol Pathol. 2024 Jun; 137:104903.
- Turko R, et al. Noncoding RNA Res. 2025 May 5;13:131-152.
- Petriv OI, et al. Proc Natl Acad Sci U S A. 2010 Aug 31;107(35):15443-8.
- Sun L, et al. Blood Sci. 2025 Mar 17;7(2): e00209.
- Jehn, J. et al. Sci Data 11, 164 (2024).
- Kirschner MB, et al. Front Genet. 2013 May 24; 4:94.
- Kim Y, et al. Mol Cell. 2012;46(6):893–5.
- Brown, R.A.M., et al. BMC Biotechnol 18, 16 (2018).
- Lederer T, et al. Genes (Basel). 2024 Apr 16;15(4):498.
- Brunet-Vega A., et al. Anal. Biochem. 2015 ;488:28–35.
- Urbizu A. et al. Int. J. Mol. Sci. 2023 ;24:2386.
- Schindler P., et al. Cancer Cytopathol. 2018; 126:353–363.
- Bhati A., et al. Anal. Biochem. 2021; 624:114182.
- Pritchard C.C., et al. Nat. Rev. Genet. 2012 ;13:358–369.
- Wright, K., et al. Sci Rep 10, 825 (2020).
- Ramón-Núñez LA, et al., PLOS One. 2017 Oct 27;12(10): e0187005.
- Hu, WP., Chen, YC. et al., Sci Rep 10, 21132 (2020).
- Mestdagh P, et al. Nat Methods. 2014 Aug;11(8):809-15.
- Veryaskina YA, et al. Med Princ Pract. 2022;31(4):322-332.
- 機能ゲノム学(第6回)
- マイクロRNA測定技術の最近の動向 東レリサーチセンター
- 内在性コントロールの選択 | Thermo Fisher Scientific - JP
- Faraldi, M. et al. Sci Rep 9, 1584 (2019).
- D'Alessandra Y, et al. Biomedicines. 2022 Jun 8;10(6):1354.
- Cai, S. et al. Nat Commun 12, 3515 (2021).
- Duy J, et al. BMC Genomics. 2015 Feb 18;16(1):95.
- Zununi Vahed S, et al. Bioimpacts. 2016;6(1):25-31.
- Moret I, et al. PLoS One. 2013 Dec 23;8(12):e82753
- Llorens-Revull M, et al. Int J Mol Sci. 2023 Jul 29;24(15):12183.
- Alexander, Sprygin, et al. BMC research notes 12.1 (2019): 371.
- Konno M, et al. Nat Commun. 2019 Aug 29;10(1):3888.
- Udono H, et al. ACS Nano. 2024 Jun 18;18(24):15477-15486.
- Wei W, et al. Anal Chem. 2025 Oct 21.
- Datinska, V. et al. Sci Rep 11, 22736 (2021).
2026.03