SOLUTION
検査室支援情報
検査の樹 -復習から明日の芽を-
19 期待が湧くマイクロRNA診断検査
Ⅰ:急拡大するマイクロRNA診断検査の基礎
はじめに
生体液を用いた診断法は、高度な分子生物学的分析技術の開発・普及および分析機器等の急速な進展により、2010年代に入りリキッドバイオプシー(液体生検:Liquid biopsy)と再定義された。近年、リキッドバイオプシーは高度化した分子生物学的分析法の応用に伴い、さらにはAIや機械学習等の進展により、少量の低侵襲体液から多種多様な分析・解析情報が取得できるようになった。この様な分析・解析の大系化により、早期臨床診断、診断確率、予後推定などの精度が高まり、新規治療法の開発、さらには、これまで診断が困難であった疾患の診断等々にと、その応用は急拡大化の傾向が見られる。
リキッドバイオプシーでは、血液や尿、唾液、脳脊髄液、便など低侵襲性生体液サンプルを分析・解析し診断を行う。現行のリキッドバイオプシーでは、血中循環腫瘍細胞(CTC)、血中循環腫瘍DNA(ctDNA)、血中循環腫瘍RNA、細胞外小胞などの解析を主体として行われている。図1にリキッドバイオプシーの概略図と、その遺伝子成分が血液中に現れる様子を示した。
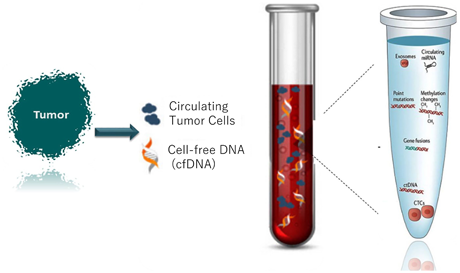
図1 液体生検の概略図と、その遺伝子成分が血液中に現れる様子
Aghamir SMK, et al., Epigenet Insights. 2020 Feb 28;13:2516865720904052.から引用
執筆時点において国内で薬事承認および保険適応を受けているのは、コバスEGFR変異検出キットv2.0、Archer METコンパニオン診断システム、OncoBEAM RAS CRCキット、FoundationOne Liquid CDxの4種類があるが、さらに、多くの新規手法の開発・基礎研究、診断困難な疾患への応用など研究開発は活況であり、その成果は枚挙に暇が無いほどである。この様に優れた利点の多いリキッドバイオプシーであるが臨床導入には課題も残っており、堅実な論理と技術の習得が求められている。本稿では、リキッドバイオプシーの中でも近年急速な進捗を遂げているノンコーディングRNA(ncRNA)の一群であるマイクロRNA(miRNA)について、「期待が湧くマイクロRNA診断検査」と題し、『Ⅰ:急拡大するマイクロRNA診断検査の基礎』、『Ⅱ:マイクロRNA診断検査:間近な臨床応用とその課題』の2部に分けて解説する。尚、参考文献・資料が多いためⅠ部とⅡ部とに分割して記載した。
1.ノンコーディングRNA(ncRNA)とは
<1文字違いの略号や類似の略号にご留意ください。また、関連用語の説明を文中に<>で記載した。>
DNAに格納された生物の生態遺伝情報は、DNAからmRNAに転写され、タンパク質へと翻訳される。このDNA⇒mRNA⇒タンパク質へと一方向に伝達される分子生物学の基本原則をセントラルドグマと云う。しかし、DNAから転写されたmRNAの遺伝情報が全てタンパク質に翻訳されるのではない。FANTOM(Functional Annotation of the Mammalian genome)プロジェクトとENCODE(Encyclopedia of DNA Elements)などの大規模な国際コンソーシアムは、パーベイシブ転写(pervasive transcription:DNAの80%がRNAに転写されるが、そのRNAのわずか1.5%がタンパク質に翻訳される)を説明した(Carninci et al. 2005[1] ; Hangauer et al. 2013[2])。この様に真核生物のゲノムの約90パーセントは転写されるが、タンパク質に翻訳されるのはわずか1~2パーセントと云われている[3][4]。
DNAから転写されたRNAでタンパク質に翻訳されないRNAをノンコーディングRNA(non-coding RNA:ncRNA)と総称する。ncRNAは、タンパク質に翻訳されない機能的なRNA分子群であり、ハウスキーピングncRNAと機能的ncRNA群とに分かれる。ハウスキーピングncRNAの代表的な分子群としては、量的に豊富なtRNAとrRNAがある。機能的ncRNAは、小分子群(数ntから200nt未満)のmiRNA、siRNA、piRNAなどと、長鎖群の長鎖非コードRNA(200ntを超え数キロベースにおよぶことがある):long noncoding RNA(lncRNA)に分類され、Xist, HOTAIRや環状RNAなどが含まれる。
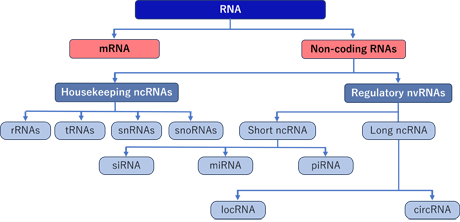
図2 さまざまな種類のRNAと主要な非コードRNA
Loganathan T; Funct Integr Genomics. 2023 Jan 10;23(1):33.より引用
これら2つのグループはお互いに異なる機能を持つ。主な非コードRNAの機能と概要を表1に一覧化した。
表1 非コードRNAとその機能の概要
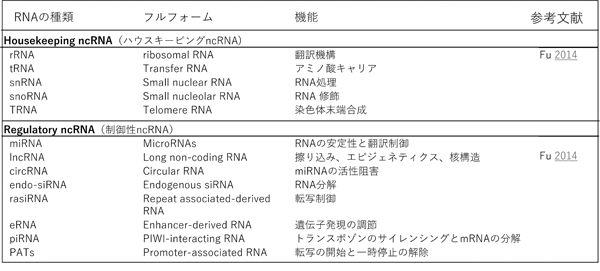
参考文献 Fu X-D. Non-coding RNA: a new frontier in regulatory biology. Natl Sci Rev. 2014;1(2):190–204.
Loganathan T, et al., Funct Integr Genomics. 2023 Jan 10;23(1):33.から引用し一部改変
<Housekeeping ncRNA(ハウスキーピングncRNA)とは、恒常的に発現して転写や翻訳に関わるノンコーディングRNA(ncRNA)です。>
ncRNAは、エピジェネティクス分野において盛んに研究が行われており、真核生物は、RNA処理、トランス誘導、DNAメチル化、インプリンティング、RNA干渉(RNAi)、転写後遺伝子サイレンシング、クロマチン修飾、遺伝子編集、スプライシング、用量補償、遺伝子調節機構、転写遺伝子サイレンシングのためのより高度で複雑なシステム機構を持っている。
発生、代謝、神経系の機能、さらには、さまざまな疾患の発症や進行への関与、他のRNA活性の調節、タンパク質の翻訳後修飾など広範囲な関与が解明されて来た。本稿のテーマであるマイクロRNA(miRNA)はこのncRNA群に属する[5]。
ncRNA の研究は、健康と疾患におけるその機能を理解するために不可欠である[6]。
多くの研究者により多数のノンコーディングRNA(ncRNA)が発見され、ヒト細胞中に存在するRNAの7割がncRNAであることがわかり、遺伝子発現の調節機構におけるncRNAの重要性と多様な機能が続々と報告されている。この様に、現在ncRNAは盛況な研究分野の一つと云える。恰も2024年のノーベル生理学・医学賞は、アメリカ・マサチューセッツ大学のビクター・アンブロス教授と、ハーバード大学のゲイリー・ラブカン教授が『マイクロRNAの発見および転写後の遺伝子発現の調節における役割の解明』との功績で授与された。
これらの分子に対する理解は飛躍的な向上を遂げているが、タンパク質構造と分子がどのように結びついているかについては未だ充分な解明には至っていない。
生物は生涯同じゲノムDNAを使ってライフステージを変化させていく。一卵性双生児に見られるように同じゲノムDNAからスタートしても後天的な要因(環境因子)により、DNAやヒストンタンパク質の化学修飾などの諸種の要因によりエピジェネティック制御の差異を生む。エピジェネティック制御の異常はがんや神経疾患、循環器疾患、代謝疾患、アレルギー、慢性炎症性疾患、免疫疾患など多くの疾患において発症・進行との関連性が認められている。エピジェネティック異常は、DNAの一次構造には影響を与えないため異常タンパク質の創生は無いが遺伝子発現の調節に強く変調をきたしてくる。近年、諸種疾患における遺伝子発現機構の解明により、ncRNAの複雑多様な関与と機能が判明しつつありその重要性の認識と共に診断、治療、予後推察への応用研究が盛んに行われている。
ncRNAは、基本的にはすべてDNAから転写されている。現在の生物学的知識ではDNAから転写されたものでないものは存在しないとされている。タンパク質に翻訳されないncRNAは、遺伝子発現の調節や個別細胞の機能発現に重要な役割を発揮している。転写により派生したncRNAは、各々固有の機能を有し、クロマチン構造/エピジェネティックメモリ、転写、RNAスプライシング、編集、翻訳、ターンオーバーなど、生理学および発達などの各時点において複雑かつ多種多様な機能を他の分子と連携しながら発揮し、様々なレベルの遺伝子発現を制御する。タンパク質に翻訳されない機能的なncRNAが転写されるDNA配列はRNA遺伝子と呼ばれることもある。
ncRNAは生体において交絡因子と高度な連携の基に多様な調節機能を発揮する。大量なncRNAとしては、生体に豊富に存在し、機能的にも重要な、転移RNA(tRNA)とリボソームRNA(rRNA)とがある。小分子RNA群としては、マイクロRNA(miRNA)、低分子干渉RNA(siRNA)、Piwi相互作用RNA(piRNA)、核小体小RNA(snoRNA)、核小RNA(snRNA)、小型カハール小体特異的RNA(scaRNA)およびsmall cytoplasmic RNA(scRNA)などがある。また、200ntを超える長鎖群としては長鎖非コードRNA:long noncoding RNA(lncRNA)、X不活性特異的転写産物(Xist)、HOX転写アンチセンスRNA(HOTAIR)などやRNAの5’末端と3’末端を共有結合で閉じた環状構造を持つ環状RNA(circRNA)などがある。多くの種類の環状RNAは、タンパク質をコードする遺伝子から生じる。また、一部の環状RNAはペプチドをコードすることが示されている[7][8][9]。
1-a. 大量なノンコーディングRNA
1-a-ⅰ. 転移RNA(Transfer RNA:tRNA)アミノ酸キャリア
tRNAは、DNAから転写され、通常76-90nt(真核生物の場合)のRNAからなるアダプター分子であり、アミノ酸をリボソームに運び、遺伝情報を含むmRNAとタンパク質のアミノ酸配列とを物理的に結びつける役割を担いタンパク質合成の過程をサポートする。
1-a-ⅱ. リボソームRNA(Ribosomal RNA:rRNA)翻訳機構
DNAから転写したRNAで、細胞内小器官リボソームの主要な構成要素でありmRNAの情報を基にアミノ酸を結合させるタンパク質合成の翻訳装置として機能する。
リボソームは、RNAとタンパク質からなる巨大な複合体で、タンパク質の合成(翻訳)を担っている。リボソームは大小2つのサブユニットから構成されており、その中心部にはRNA分子、表面にはタンパク質が結合している。RNAとしては生体内でもっとも大量に存在する(7-8割程度)。
1-b. 主なsmall non-coding RNAs(snRNAs) 小分子非コードRNA
1-b-ⅰ. マイクロRNA(microRNA:miRNA)RNAの安定性と翻訳制御、細胞間コミュニケーション
17~24ntの一本鎖RNAで、RNA誘導サイレンシング複合体(RNA induced silencing complexes; RISC(リスクと読む))に取り込まれて機能する。miRNAは、mRNAの転写産物の相補配列と部分的に結合し、mRNAの翻訳を阻害することでターゲットのタンパク質発現を抑制する。がん、心血管疾患、神経変性疾患など多くの疾患の診断や予後のバイオマーカーおよび治療に利用されている。
1-b-ⅱ. RNA低分子干渉RNA(Small interfering RNA:siRNA)遺伝子発現の抑制、ウイルス感染の防御
siRNAはダイサーによって処理される長い線状dsRNAから派生した20~24nt長の分子で、二本鎖RNAである。miRNAと同様、RNA誘導サイレンシング複合体(RNA induced silencing complexes; RISC)に取り込まれて機能する。最終的には、RISC内でヘリカーゼによって1本鎖RNAとなる。
siRNAは、mRNAの転写産物の相補配列と全体が結合し、特定のmRNAを分解させるよう誘導することで、タンパク質の遺伝子発現を抑制する。
siRNAは、RNA干渉(RNAi)を介して遺伝子サイレンシング(遺伝子発現抑制)を行い、ウイルス感染や遺伝子発現の調節を行う[10][11]。
<miRNAとsiRNAは同じmRNAサイレンシング作用を示すがその機能的違いは>
miRNAは、mRNAの配列と6-8塩基が相補的であれば結合できる。一方、siRNAは、mRNAの配列が完全に相補的でないと結合しない。
どちらもmRNAに結合し、タンパク質の発現を抑制する機能は同じであるが、上記の結合の違いから、miRNAは1種類で複数のmRNAの転写を阻害し、siRNAはターゲット特異的にmRNAの転写を阻害する。また、1種類のmRNAは複数のmiRNAによって制御されている。
1-b-ⅲ. Piwi-総合作用 RNA(Piwi-interacting RNA:piRNA)トランスポゾンのサイレンシングとmRNAの分解
piRNAは、24~31ntの1本鎖RNAで、5'末端にウリジン、3'末端に2'-O-メチル修飾を持っている。piRNAは、RNA干渉プロセスで重要な役割を果たすアルゴノートファミリーのPiwiタンパク質と複合体を形成する。さらに、哺乳類とハエのPiwi/piRNA複合体は、生殖細胞発生中の転移因子の制御に関連し、生殖細胞系および体細胞のトランスポゾンの発現を抑制する。piRNAと結合したPiwiタンパク質は、piRNAと相補的配列をもつトランスポゾンRNAを認識し切断する。piRNAは、生殖細胞においてトランスポゾンの抑制に重要な役割を果たし、遺伝的安定性を維持し、ゲノムの保護に寄与する(生殖細胞の保護)[12][13]。
1-b-ⅳ. 小核小体RNA(Small nucleolar RNA:snoRNA)RNA修飾
核小体小RNA(snoRNA)は、60~300ntの長さで真核細胞の核小体に広く存在し、rRNAのメチル化や偽ウリジン化を行い、リボソームの機能を調節する。さらにtRNAおよびmRNAの修飾へも関与していることが示されている。腫瘍促進性snoRNAや腫瘍抑制性snoRNAを含む多数のsnoRNAが腫瘍で調節不全になっている。リボソームタンパク質と結合しリボソームのアセンブリにブレーキをかけることで、細胞老化に伴う細胞増殖停止に関わっている。snoRNAには、Box C/DとBox H/ACAの2つの主要なタイプがある。
1-b-ⅴ. 核小RNA(Small nuclear RNA:snRNA)RNA処理
snRNAの平均的な長さは約150ntであり、真核細胞のカハール小体内に多く見られる。主要な機能は、核内のmRNA前駆体(hnRNA)のプロセシングである。スプライシングに関与するRNAで、スプライソソームの構成要素である。前駆体mRNA(pre-mRNA)のスプライシングを行い、成熟mRNAの生成に寄与する。また、転写因子の調節やテロメアの維持にも作用することが示されている[14]。
1-b-ⅵ. Y RNA DNA複製やRNAの安定性、細胞ストレス応答などに関与
Y RNAは100±20ntの特徴的なステムループ二次構造に折り畳まれ、単一の膨らんだシトシンを特徴とする。Y RNAは短い非コードRNAの一種です。合計で4つの異なる転写産物、つまりYRNA1、YRNA3、YRNA4、YRNA5が区別される。これらはRo60リボ核タンパク質粒子の構成要素であり、複製開始タンパク質(複製起点認識複合体やクロマチンなど)との相互作用によりDNA複製に積極的な役割を果たす。5'側と3'側に保存された配列を持ち、Roタンパク質とLaタンパク質が結合している。ヒトにはhY1、hY3、hY4、hY5という4つのY RNAがある[15][16]。
1-c. 主な長鎖分子非コードRNA
1-c-ⅰ. 長鎖非コードRNA(long noncoding RNA:lncRNA)刷り込み、エピジェネティクス、核構造
lncRNAは、200ntを超え(500nt以上との意見もある)、多様な機能を持ち、ncRNAの大部分を占める。ncRNAは塩基の長さによってmiRNAなどの短いncRNAと長いncRNA(lncRNA)との2つの主なクラスに分けられる。lncRNAは、転写後にスプライシング、アデニル化などの方法で修飾される。lncRNAは他の分子と関連して幾つかの生理学的プロセスを調整する。その機能不全は癌や感染症などのいくつかの病状に影響を及ぼす。lncRNAは、染色体構造の調整、転写、スプライシング、メッセンジャーRNA(mRNA) の安定性、mRNAの可用性、翻訳後修飾など、遺伝情報の流動を制御することができる。lncRNA は、配列と二次構造の両方に応じて、DNA、mRNA、miRNA、およびタンパク質の相互作用ドメインを示す[17]。
既知のヒトlncRNAの数は劇的に増加しているが、それらの注釈は不十分なため、それらの機能的重要性をより深く理解すると共に、それらの複雑な機能分子メカニズムを解明することは大きな課題と云える。
lncRNAの体系的なキュレーション(精選)を特徴とする、キュレーションされたヒトlncRNAのノーレッジベースのLncBook(http://bigd.big.ac.cn/lncbook)が紹介されている。現在のバージョンでは、LncBookには270,044のlncRNAが収められ、3762のlncRNAと機能の関連付けを持つ1867の注目されているlncRNAが含まれている。また、発現、メチル化、ゲノム変異、lncRNAとmiRNAの相互作用からの豊富なマルチオミックスデータも統合されている[18]。
lncRNAは、生合成部位によって、ⅰ)intergenic lncRNAs(lincRNAs)[19]、ⅱ)intronic incRNAs、ⅲ)antisense(aslncRNA or natural antisense transcripts、NATs) [20]、ⅳ)Bidirectional lncRNAs、ⅴ)enhancer RNAs(eRNAs)に分類される。
lncRNAの疾患との関連例を挙げると
神経変性疾患:lncRNAは、アルツハイマー病やパーキンソン病などの神経変性疾患に関与する。特定のlncRNAは、神経細胞の生存や機能に影響を与える[9][21]。
がん:lncRNAは、がん細胞の増殖や転移に関与し、がんの進行を促進することがある。例えば、HOTAIR(HOX Transcript Antisense Intergenic RNAの略でlncRNAの一種)は乳がん、大腸がんの進行に関連している[22][23]。
lncRNAは、 遺伝子発現の調節、クロマチンリモデリング、転写後の調節など、多岐にわたり役割を果たす[23]。
lncRNAは、転写因子やクロマチン修飾因子と相互作用し、特定の遺伝子の転写を促進または抑制する。例えば、lncRNAはプロモーター領域に結合し、転写因子のアクセスを妨げることがある。ヒストン修飾やDNAメチル化などのエピジェネティック修飾を介しても遺伝子発現を調節する。これにより、細胞の分化や発生過程における遺伝子発現パターンが制御される。また、RNA-RNA相互作用として、lncRNAは、他のRNA分子と相互作用し、その安定性や機能を調節する。例えば、lncRNAはmiRNAのスポンジ(スポンジの様にmiRNAを吸取りmiRNAの作用を抑制する。)として機能し、miRNAのターゲットmRNAへの結合を妨げる。これらの機能により、miRNAとlncRNAは細胞の機能や遺伝子発現の調節に重要な役割を果たしている。さらに、核内の特定の構造(例:核小体)の形成に関与し、遺伝子発現の調節に関与する。
1-c-ⅱ. 環状RNA(circular RNA :circRNA)miRNAの活性を阻害
circRNAは、がんの進行に関与し、特定のcircRNAはがんの診断や治療のターゲットとして研究されている。circRNAは、環状構造を持つRNAで、エクソンやイントロンから生成される。miRNAのスポンジとして機能し、遺伝子発現の調節に関与する[23]。
<circRNA:miRNAのスポンジとして機能する>
miRNAスポンジとは、miRNAはmRNAと結合して遺伝子発現を抑えることが知られているが、lncRNAや巨大な環状RNA(circRNA)は、miRNAスポンジとして機能し、このmiRNAをスポンジのようにどんどん吸い取って、miRNAの作用を阻害する機能を示し、遺伝子発現を変化させる[24]。
ncRNAは、それぞれ異なる機能を持ち、細胞内で他の分子と協調しながら、遺伝子発現の調節や細胞機能の維持に重要な役割を果たし、さまざまな疾患の発症や進行に深く関与している。一例を挙げると環状RNAが膵癌組織で高発現するのみならず、膵癌患者およびその前癌病態にある患者の血液からも高頻度に検出されることが報告された[25]。今後の展開に期待が持たれる分子群である。
2.マイクロRNAとは
本題であるマイクロRNA(miRNA)は18~25ntサイズ[26]の小さなncRNAの一種で、1本鎖RNA分子である[27]。多くのmRNAの機構を分解もしくは翻訳を遅らせる、またはその両方によりmRNAを制御する。短鎖非コードRNAの膨大なファミリーである。
真核生物において遺伝子の転写後発現調節に深く関与し、重要な役割を果たす。miRNAはその標的mRNAに対して不完全な相同性をもって結合し、miRNAは標的遺伝子の3'UTRを認識して、標的mRNAを不安定化するとともに翻訳抑制を行うことでタンパク質産生を抑制する。miRNAが介する転写抑制は、発生、細胞増殖および細胞分化、アポトーシスまたは代謝といった広範な生命現象に深く関わっている[28]。
miRNAは、がん、心血管疾患、免疫疾患などさまざまな疾患の分子病態において重要な役割を果たしている。血液や唾液、尿など多種の生体液に含まれ、がんなどの疾患の種類によってその種類や量が変動することが明らかになってきた。このため、がんの診断や治療薬としての応用に期待が持たれている。また、好都合なことにmiRNAは唾液、尿、母乳、血液などの生体液中に含まれかつ安定している。細胞外miRNAは、アルブミン、高密度リポタンパク質(HDL)などにロードされるか、小胞の外側でAGO2タンパク質に結合する、もしくはエクソソームや微小小胞に内包され、分解を防ぎ安定性を確保する[29]。
動物では、miRは遺伝子発現の転写後阻害剤として機能するが、miRNAと5' UTR、コード配列、遺伝子プロモーターなどの他の領域との相互作用も報告されている。また、特定の条件下では、miRNAは翻訳を活性化する、さらには転写の調節もする。miRNAと標的遺伝子の相互作用は動的であり、miRNAの細胞内位置、miRNAと標的mRNAの存在量、miRNA-mRNA相互作用の親和性など、多くの要因に依存する。また、miRNA はエクソソームなどの小胞に内包され、細胞外液に放出、もしくはアルゴノートや、アルブミン、HDLなどのタンパク質に結合して標的細胞に輸送される。細胞外 miRNA は、細胞間コミュニケーションを仲介する化学伝達物質として機能するとも考えられている。
この様に小分子ながら広範囲な生体において細胞内遺伝子発現を調節する多彩な機能を発揮するマイクロRNA(miRNA)の研究や解析(マイクロRNA遺伝子のバイオインフォマティクス:生物情報学もしくは生命情報科学)を総称しmiRNomics[30](ミルノミクス)と云う。また、細胞、組織、または生物で発現するマイクロRNA(miRNA)の集合をmiRNome(ミルノーム)と云う。例えば、ヒトのがんのmiRNome、造血幹細胞と樹状細胞のmiRNomeなどと用いる。
3.マイクロRNA(miRNA):生合成、形態、機能
3-a. マイクロRNA(miRNA)の生合成
miRNAは、DNAから転写されたpri-miRNAからpre-RNAを経て成熟miRNA(mature-miRNA)へと生合成する。mature-miRNAはRNA誘導沈殿複合体(RNA-induced silencing complex:RISC(リスクと読む))に取込まれ、標的mRNAと結合してmRNAの分解を制御する。さらに、細胞外miRNAは体内を循環し、細胞間コミュニケーションの化学伝達物質とも考えられている。miRNAの標準的な生合成プロセスの概略を図3に示した。
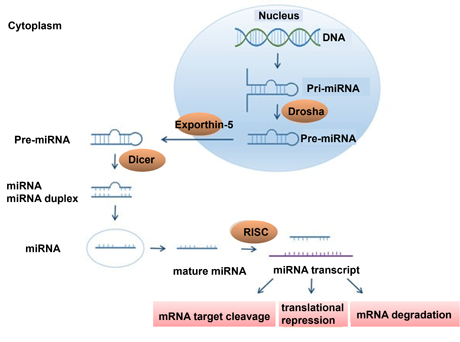
図3 miRNA の生合成プロセス
Liu J, et al; Cells. 2022 Feb 7;11(3):572.より引用
<転写物⇒ pri-miRNA⇒ pre-miRNA⇒ 核外輸送⇒ mature-miRNA⇒ RISC形成>
miRNAの生合成過程は、DNAからRNAポリメラーゼIIによって転写された転写物のRNA配列内で相補な部分は、内在的に結合して2本鎖となり、最終的にヘアピンループ型となる(pri-miRNA (primary miRNA、初期転写産物))[31][32]。pri-miRNAは数百~数千nt長の長鎖RNAで、5’末端側にキャップ構造(5'-cap:7mGppp、7-methyl guanosine)が形成され、3'末端側にはポリAテール(3'-poly-A tail:AA...A、 polyadenosine)が付与される[33]。pri-miRNAの生合成⇒核内でのRNase IIIファミリーの酵素であるDrosha(ドローシャ)によって分子の一部を切断し、70〜100nt数のヘアピン状の前駆体miRNA(pre-miRNA:precursor miRNA、成熟miRNAの前駆体)を作る[34]。(pre-miRNA)の生合成⇒pre-miRNAはExportin5を介して核より細胞質へと移送される核外輸送⇒細胞質に放出された後、RNase IIIファミリーに属するDicerによって切断され、成熟miRNA(mature-miRNA)2本鎖となる。これらの断片は約20–25ntの長さであり、3'末端に2塩基のオーバーハング(突出)が存在する。miRNA duplex(mature-miRNA)の産生⇒RISC形成の各ステップからなる。
ほとんどの場合、miRNAは標的mRNAの3'非翻訳領域(3' UTR)と相互作用して、mRNAの分解と翻訳抑制を引き起こす。
RISCは、タンパク質複合体リボヌクレオタンパク質であり、転写や翻訳段階において遺伝子サイレンシングを行う[35]。RISCはmiRNAなどの一本鎖RNA断片や二本鎖のsiRNAを利用して、遺伝子調節機能を発揮する[36]。相補的なmRNAが見つかると、RISCの構成タンパク質のアルゴノート(Argonaute)がmRNAを切断し遺伝子の翻訳反応を阻害する[37]。この過程は真核生物でみられRNA干渉(RNAi)と呼ばれる。
miRNAやsiRNAは、RISCに組込まれmRNAを分解標的とするガイド配列として作用する[38][39]。
2本鎖のmiRNAはアルゴノートタンパク質(RNA誘導サイレンシング複合体を構成する触媒タンパク質)によって選択され、RISCに取り込まれる[40][41]。RISCに取り込まれた2本鎖miRNAはRISC中で解かれ、2つの1本鎖miRNAとなる[42]。
<1本鎖になったmiRNAはガイド鎖とパッセンジャー鎖に分かれる。ガイド鎖はアルゴノートタンパク質に組込まれ、遺伝子サイレンシング機能を発揮する。パッセンジャー鎖はRISCのプロセス中に分解される。>
RISCの主要なタンパク質であるアルゴノート2(AGO2)、SND1、AEG-1は、遺伝子サイレンシング機能に重要な役割を果たす[43]。
mature-miRNAの塩基配列の5'-末端側より2番目~8番目までの7塩基は、seed配列と呼ばれ[44]、この配列と相補的な配列をもつmRNAは、mature-miRNAの標的として強く認識される[45]。
3-b. マイクロRNAの命名
miRNA命名法の詳細については、参考文献[46][47][48][49]をご参照ください。
マイクロRNA(miRNA)の命名規則の概要は以下の通りである。
マイクロRNA(miRNA)は、「mir」という接頭辞と固有の番号を使用して命名される。
- (1)種名:動物のmiRNAにはダッシュ記号が付き、3文字の接頭辞で種を示す。
ヒト(hsa)、マウス(mmu)。例 hsa-miR-101:ヒトのmiRNA - (2)構造のタイプを定義:成熟miRNAには「miR」、pre-miRNAには「mir」が使われ、大文字と小文字で区別する。
- (3)塩基配列の登録番号を定義する:miRNAは連続した番号で命名され、同定された順に番号が付く。類似した配列の場合、番号の後ろに小文字のアルファベットを付ける。
- (4)生成過程の由来を定義する:異なる遺伝子座を由来とする場合、数字で区別する。同じ前駆体を由来とする場合、5’末端側の鎖を5p、 3’末端側の鎖を3pとして区別する。定義しない場合もある。
- (5)miRNAの名称を定義する:(1)~(4)で定義した因子をハイフンでつなげる。
miRNAの具体的名称と主な相違点を例示する。(例示miRNAはランダムに選出した。)
☆hsa-miR-101:ヒトのmiRNA
☆miR-124:miR-456より前に発見されたmiRNA
☆mir-33:pre-miRNA
☆miR-340-3p, miR-340-5p
miR-340-3p:pre-miRNAの3’末端から生成される鎖
miR-340-5p:pre-miRNAの5’末端から生成される鎖
☆miR-200a-3p, miR-200b-3p, miR-200c-3p(miR-200ファミリー)
miR-200a-3p:染色体1に位置する
機能:上皮間葉転換(EMT)の抑制、がん細胞の転移を防ぐ、がんの抑制因子
miR-200b-3p:染色体1に位置(miR-200a-3pの近く)する
機能:EMTの抑制に関与し、がん細胞の遊走と浸潤を抑え、miR-200a-3pと似た
機能を持つが、標的遺伝子や効果の強さに違いがみられることがある
miR-200c-3p:染色体12に位置する
機能:EMTの抑制に関与、特にZEB1やZEB2などのEMTに関与する転写の発
現を抑え、上皮細胞の特性を維持する等があげられる。
この他には配列変異(isomiR)などの注釈が付記される。
Desvignesらは、2015年にmiRNAの命名に遺伝的起源、生合成経路、および配列変異を考慮した命名規則の見直しを提案した。提案での主な目的は、miRNAの命名規則を改善し、科学コミュニティ全体での一貫性と明確さを高めることを求めた。今では提案に沿った改善が遂行されている。また、この時Mirror-MiRsの記述法も提案されている[50]。
さらに、miRNAの種類やSNPの影響についても改善が望まれる。例えば、「SNP rs12402181がmiR-10b-5pの機能に影響を与える」といった具体的な記述が必要である。
*但しrs番号(Reference SNP ID number)は各々のSNPに定義した番号でありSNPの遺伝子における位置を示しているものではない。rsは常に小文字である[51]。
現在までに動物、植物を含む多くの生物種から数万のmiRNAが発見されている。ヒトゲノムには約2,600個の成熟マイクロRNA(miRNA)が含まれるとされている。但し、データベース内のmiRNA数は絶えず増加しているため正確な数字の特定は困難である。また、2019年miRNAの検証により、真のヒト成熟miRNAが2,300個あると推定された[52]。
3-c. マイクロRNA(miRNA)の機能
mRNAの翻訳抑制と分解
【miRNAの機能】
遺伝子の発現制御ネットワークを巧みに調節する
●翻訳抑制、mRNA切断、脱アデニル化など、さまざまな形式で遺伝子発現を低下させる
『 miRNAはmRNA分子の相補配列と塩基対を形成し、[53]次に、以下の1つ以上のプロセスによりmRNA分子をサイレンシングする[54][55]。
●mRNA鎖を2つに切断する。
●ポリ(A)テールを短くすることでmRNAを不安定化させる。
●mRNAからタンパク質への翻訳を減らす。
ヒトを含む動物の細胞では、miRNAは主にmRNAを不安定化させて作用する[55][56]。
miRNAの作用機序としては次の9つが考えられている。
● Cap-40S開始阻害、● 60Sリボソームユニット結合阻害、● 伸長阻害、● リボソームの脱落(早期終結)、● 翻訳に伴って起こる新生タンパク質の分解、● P-bodyへの隔離*、● mRNAの分解(不安定化)、● mRNAの切断、● マイクロRNAを介したクロマチン再構成による転写阻害とそれに続く遺伝子サイレンシング。microRNA Wikipedia: microRNA - Wikipediaから抜粋し改変』
*<P-body(Processing body)は、RNAの分解に関与するタンパク質を多く含むRNA顆粒で細胞質に存在する。粒子状構造で、miRNAによる翻訳抑制、ポリAの短縮によるRNAの分化、RNA分解の中心的役割などの機能を有し、RNAの貯蔵や分解など、さまざまな機能を持つ。>
4.マイクロRNAの作用機序、循環の概要
4-a. マイクロRNA(miRNA)の機能の概要
miRNAは、主に以下のような機能を行う。
- ⅰ. mRNAの翻訳抑制:
miRNAは、ターゲットmRNAの3’UTR(非翻訳領域)に部分的に相補的に結合する。
この結合により、mRNAの翻訳が抑制され、ターゲットタンパク質の発現が減少する。 - ⅱ. mRNAの分解:
miRNAがmRNAに完全に相補的に結合すると、mRNAは分解される。
これにより、ターゲットmRNAの量が減少し、遺伝子発現が抑制される。 - ⅲ. RNA誘導サイレンシング複合体(RISC):
miRNAはRISCに取り込まれ、RISCがターゲットmRNAを認識して結合する。
RISCは、mRNAの翻訳抑制や分解を促進する
4-b. miRISCを介したマイクロRNAによる遺伝子サイレンシング
『miRNA誘導サイレンシング複合体(miRISC)は、miRNAのガイド鎖とAGOで構成されている[57]。miRISCの標的特異性は、miRNA応答要素(MRE:microRNA recognition element)と呼ぶ、標的mRNA上の相補配列との相互作用による。MRE相補性の程度により、標的mRNAのAGO2 依存的な切断もしくは、miRISCを介した翻訳阻害と標的mRNA の分解かがわかる。完全に相補的なmiRNA:MRE相互作用は、AGO2エンドヌクレアーゼ活性を誘導し、mRNA標的を切断する[58] 。しかし、この相互作用はAGOとmiRNAの 3'末端との連結を不安定にし、分解を促進する[59] [60]。
動物細胞では、miRNA:MRE相互作用の大部分は完全には相補的ではない。ほとんどのMREは、ガイドmiRNAに対して少なくとも中央のミスマッチを含み、AGO2エンドヌクレアーゼ活性を妨げる。結果的に、 AGO2は、非エンドヌクレアーゼAGOファミリーメンバー(ヒトのAGO1、3、および4)と同様に、RNA干渉のメディエーターとして機能する。多くの場合、機能的なmiRNA:MRE相互作用は5'シード領域(ヌクレオチド2〜8)を介して発生する[61][62]。(O'Brien J, et al., Front Endocrinol(Lausanne). 2018 Aug 3;9:402.)から抜粋引用し一部改変』
mRNAの翻訳抑制には、microRNA(miRNA)やCRISPR-Casシステム、4EHPなどのタンパク質などが関与する。
【microRNA(miRNA)による翻訳抑制】
●小分子RNAのmiRNAは、標的とするmRNAの翻訳を抑制する
●RISCと呼ばれるRNA-タンパク質複合体を形成することで機能を発揮する
●発生や分化、癌などの疾患と深く関与する
【CRISPR-Casシステムによる翻訳抑制】
●CRISPRδと呼ばれるシステムが、さまざまなmRNAの翻訳を抑制する
●4EHPと呼ばれるタンパク質をdCas13タンパク質に融合させると、CRISPRδの効果が増強される
【4EHPによる翻訳抑制】
●mRNAの末端に結合する翻訳開始因子eIF4Eによく似た翻訳抑制を行うタンパク質。mRNAの5'末端のキャップ構造に結合する能力を持ち、eIF4EとmRNAの結合を阻害することで翻訳抑制する
●4EHPは、eIF4E-homologous proteinの略
また、アミノ酸飢餓によりmTOR*が阻害された場合、LARP1が活性化しTOP mRNAの翻訳が抑制されるという報告もある。
<*mTOR(エムトール、エムトア):(mammalian target of rapamycin)は、ラパマイシンがターゲットにする細胞内タンパク質で、細胞外の栄養状態や細胞内エネルギー(ATP量)等の情報を感知して、細胞成長・増殖へ結びつける上で中心的な役割を担うリン酸化酵素。mTORには2種類の複合体(mTORC1とmTORC2)が存在する。>
<miRNAの機能解析手法>
●miRNAインヒビターなどを用いて、miRNAの機能を抑制する。
●miRNA mimic(オリゴ)やpre-miRNA発現プラスミドなどを使用してmiRNAを過剰発現させる。
●mimicやインヒビターのライブラリを使用して機能性スクリーニングを実施する。
miRNAは、細胞の分化や発生などさまざまな生命現象に関与することが知られている。
4-c. miRNAの制御機能
miRNAはsiRNAと違って、複数のmRNA配列に部分相補的に結合する。miRNAは、mRNAの翻訳反応を物理的に阻害することで、さまざまな遺伝子発現を抑制する[63]。
1種類のmiRNAは、多くのmRNAの遺伝子発現調節に関わっている[64]。逆に言い換えれば、1種類のmRNAの遺伝子発現は、多種類のmiRNAによって調節されている。miRNAは、何百ものmRNAを標的とし、多くの遺伝子の発現に影響を与えることができる。
したがって、miRNAとmRNAは複雑な遺伝子発現制御ネットワークを形成していると考えられている。 つまり、miRNAは単一で機能しているのではなく、ほかの種類のmiRNAや他のncRNAと協力することで、複数のmRNAの遺伝子発現を抑制している[65]。 このようにして、miRNAは制御機能のバランスを保ち、生物の恒常性を維持している。
miRNAは、単独では機能発現できないため、競合する内因性RNA(Competing endogenous RNA:ceRNA)は、RNAが共有miRNAの争奪をめぐって競合する(制御メカニズム)。このプロセスは遺伝子発現に影響をおよぼし、がんなどのさまざまな生物学的プロセスに関連していると考えられているが、ヒトのceRNAネットワーク仮説はまだ初期段階とされている。しかし、PTENceRNAネットワーク、Linc-MD1、BRAFP1など多くの立証データが蓄積されている。miRNAは、MREに結合してタンパク質コードmRNAを抑制するlncRNA、snRNA、piRNA、またはtRNAから生成される非標準的生合成経路を取ることがある。circRNA、lncRNA、擬似遺伝子(pseudogene)などの異なるクラスのceRNAにもMREが含まれており、miRNAの結合を競合する。図4にmiRNA生合成とceRNAのネットワークの概略を図示した。
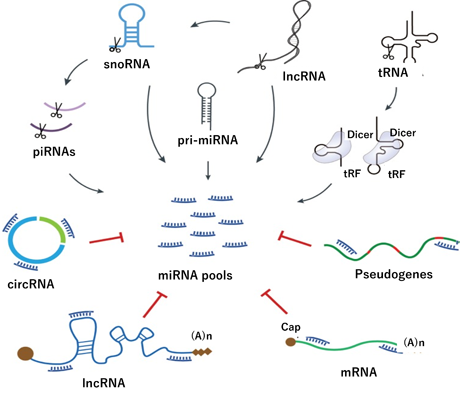
図4 miRNA 生合成と ceRNA(competing endogenous RNA) のネットワーク
Zhang P, et al.,J Integr Bioinform. 2019 Jul 13;16(3):20190027.より引用
<miRNA inhibitorの原理は>
miRCURY LNA miRNA Inhibitorsは、特定のマイクロRNA(miRNA)と結合してその働きを妨げる薬剤で、ターゲットのmiRNAと相補的な配列を持つアンチセンスオリゴヌクレオチドである。細胞に導入されると、それらはターゲットのmiRNAと強固に結合して二本鎖を形成し、miRNA自身が細胞内で相互作用するのを効果的に防止する。
4-d. 細胞外マイクロRNA
4-d-ⅰ. 生体液中のマイクロRNA
miRは細胞外液に分泌され、血液循環などによって他の細胞に送達されて、そこでも機能することができる[66]。これは、miRが細胞と臓器間のシグナル伝達および調整分子として役割を果たしていることを示す。さらに、細胞外miRNAは安定性が高い。このため、細胞外miRは優れた疾患バイオマーカーであることが強調されている[67][68]。
4-d-ⅱ. 細胞外マイクロRNA
生体液中には、細胞外miRNAの2つの集団が存在する。1つはエクソソーム、マイクロベシクル、アポトーシス小体などの小胞に内包され[69][70]、もう1つはタンパク質、特に AGO2と関連している[70][71]。細胞外miRNAに結合することがわかっているタンパク質としては、高密度リポタンパク質(HDL)[72][73]やヌクレオフォスミン1(NPM1) [29][74][75] 、アルブミン[76]などがある。小胞内または付随タンパク質とともにmiRNA が存在すると、一般的に細胞外miRNAが保護され、細胞外環境での安定性が向上すると考えられている[70]。図5にmiRNA生合成から排泄メカニズムと細胞外生存機構の概略を図示した。
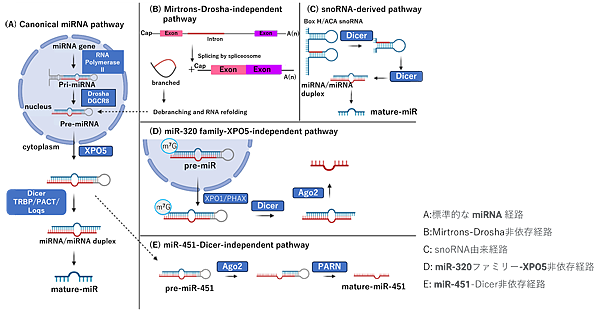
図5 マイクロRNA生合成の標準的および非標準的経路
Gregorova J, et al. Cancers (Basel). 2021 Mar 16;13(6):1333. より引用
miRNAは、多小胞体(MVB)やエクソソームを介した細胞排泄、膜剥離による微小小胞形成、AGO-2やHDLとの関連など、さまざまな方法を通じて細胞から能動的および受動的に放出される。
miRNA がエクソソームに分別される経路には、以下の4つの経路が見つかっているが、そのメカニズムは完全には解明されていない。
- 1)神経スフィンゴミエリナーゼ2依存性(nSMase2)経路で、エクソソームmiRNAの生成を促進する[77]。
- 2)異種核リボ核タンパク質(hnRNP)依存性経路で、エクソソームmiRNAの進入を制御する。
- 3)miRISC関連経路で、この経路ではmature- miRNAがAGO2および182kDaのグリシントリプトファンタンパク質(GW182)とともにRISCに組み込まれる。AGO2は主に miRNAの末端にあるUまたはAに結合し、これがmiRNA:mRNA複合体の形成を促進し、その後mRNA分子の翻訳を破壊または阻害するのに重要である[78]。
- 4)配列依存的経路は、miRNAの3'末端が関与する[79]。
4-d-ⅲ. miRNAの細胞内区画化
miRISCと標的mRNAは、粗面小胞体(rER)[80]、プロセシング(P)体[81]、ストレス顆粒(SG)[82]、トランスゴルジ体(TGN)、初期/後期エンドソーム[83]、多小胞体(MVB)[84]、リソソーム[84]、ミトコンドリア[85][86]、核[87][88]など、複数の細胞内区画に局在することが観察されている。
miRNAの存在量/局在、細胞タイプ、細胞状態、および miRNAを介した調節の相互作用については、現在も精力的に調査が進められている。
4-d-ⅳ. ターゲットmRNAとの相互作用
タンパク質、miRNA、lncRNA、mRNA、DNA、脂質などの細胞外小胞(Extracellular vesicles:EV)の成分は、腫瘍微小環境における傍分泌シグナル伝達を媒介する。細胞間コミュニケーションに参加するmature-miRNAは、多くの場合EV内でほとんどの細胞から放出され、細胞外液を介して拡散して腫瘍細胞などの遠隔標的細胞に到達する。腫瘍細胞の表現型は、標的に応じて腫瘍抑制因子またはがん遺伝子としてmRNAとタンパク質の発現を制御することによる影響を受ける[89]。
4-e. マイクロRNAの体内循環と分泌・取り込み
4-e-ⅰ. マイクロRNAの体内循環
miRNAは多くの研究により細胞外液に放出されることが実証されている。循環血液や脳脊髄液などの生体液中の細胞外miRNAは、肝臓の炎症、繊維化、がん、動脈硬化、神経性疾患など、これまでは困難とされてきた、さまざまな疾患の鑑別および疾病の早期診断、治療、予後推測などのバイオマーカーとして有益性が評価されている。
<バイオマーカーの定義は、米国の国立衛生研究所(NIH)により『病態生理学的な裏づけのもとに測定され、客観的に評価できる特性』とされている。>
細胞外miRNAはエクソソームなどに内包もしくはタンパク質と結合し標的細胞に送達され、送達細胞の活動を調節するオートクリン、パラクリン、さらには内分泌調節因子として、ホルモン様の活性を示す[90]。
がんの進行や転移においては、循環腫瘍miRNAとCTC(がん細胞)が相互に関連していることが示唆されている。miRNAは短いRNA配列でありながら細胞内の標的転写産物に結合して循環し送達した広範囲の組織・細胞において多種の遺伝子発現を正確に調節する。その特徴は、1つ以上のmRNA分子と部分的相補性を持つため複数のmRNAとに作用することである。がん細胞が血流に放出されると、特定のmiRNAも同時に放出される。このmiRNAはCTCの生存や転移能力を高める役割を果たしていると考えられており、CTCと循環腫瘍miRNAは協力してがんの転移を促進する可能性が推察される。また、miRNAの機能不全は、がん、循環器疾患、免疫疾患、精神疾患など多くのヒトの疾患との関連が解明されつつある。
4-f. マイクロRNAの分泌と取り込み
細胞外miRNAの中には、細胞傷害や細胞死などの細胞活動の副産物と見なされるものもあるが[29]、細胞外miRNAの放出は制御されたプロセスであることを示唆する証拠が増えている。エクソソームmiRNAの分泌はセラミド依存性経路によって媒介され、分泌されたmiRNAは標的細胞で成長制御効果を発揮する[91]などいくつもの機能が実証されている。
多くの研究において、細胞外miRNAが受容細胞内で生物学的機能を発揮してその活性を調節する、細胞間シグナル伝達分子として作用することも実証されている。このように、miRNAは細胞間コミュニケーションを制御する化学メッセンジャーとして作用する可能性がある。
細胞外miRNAの取り込みメカニズムは十分には解明されてはいないが、小胞に関連する細胞外miRNAは、エンドサイトーシス、貪食、または細胞膜との直接融合によって細胞内に入り、小胞から分泌されたmiRNAは細胞表面の特定の受容体によって取り込まれると考えられている[92]。さらに、HDLに関連する小胞フリーのmiRNAは、標的細胞の細胞膜にあるHDL受容体およびスカベンジャー受容体BI(SR-BI)受容体によって取り込まれる[72][73]。miRNAは、直接的な細胞間接触やギャップ結合を介して共培養細胞間を移動することも示されている[93]。これらの研究は、細胞外miRNAが複数のメカニズムを介して受容細胞と相互作用できることを示唆するが、その相互作用の特異性を決定する要因は解明されていない[94]。
5.マイクロRNAの安定性
多くの研究成果として、血漿や血清[75][95]、尿、腹水、脳脊髄液[96]、唾液[70]、母乳[97]、涙、初乳、気管支洗浄液、精液[98]、卵胞液[99]、体内貯留液、排出液物中から検出されている。細胞RNA種とは対照的に、エクソソーム内包もしくはタンパク質結合の細胞外 miRNAは非常に安定している。室温で最大4日間分解されず、煮沸、複数回の凍結融解サイクル、高pHもしくは低pHなどの過酷な条件下でも分解されない[67][95]との報告がある。
miRNA分解のダイナミクスの報告は少なく、新パルスチェイス法<生化学や分子生物学の分野で細胞内の物質の移動を追跡するために用いられる研究技術>を用いた分析によると、miRNAの半減期は不均一で、多くの種は安定した分子として振る舞う(T1/2 > 24 時間)が、パッセンジャーmiRNAや一部のガイドmiRNAなど、その他の種は急速にターンオーバーする(T1/2 = 4~14 時間)。分解率は、ゲノム構成、転写率、構造的異質性(isomiR)、ターゲット存在量などの影響を受けるようである[100]。
Oikawa等は、骨格筋に発現するmiRNAは、心臓や肝臓に発現するmiRNAと比較し、生物学的半減期が11~20時間程度と比較的短く、骨格筋に多く含まれるmiRNAは生体内で非常に不安定であり、ダイサーに依存しない方法で制御される可能性があるとしている[101]。
miRNAの生物学的半減期は数時間から数週間までさまざまであり、これらは諸種の要因によって影響を受ける。また、miRNAの種類によっても異なり、細胞周期に関与するmiRNA は他のmiRNAよりも安定性が低い。組織骨格筋では、miRNAの半減期は約10~30時間とされる。マウスの脳と心臓では、成熟したmiRNAの半減期は数週間から数か月になることがある。miRNAレベルに影響を与える可能性のあるその他の要因としては、CG含有量、結合タンパク質、mRNA:miRNA相互作用、miRNA編集、miRNAメチル化、競合する内因性RNA(ceRNA)への結合などがある。
<ceRNA(competitive endogenous RNA:競合関係にあるRNA)とは、競合関係にある複数のlncRNAやmRNAが単一のmiRNAを奪い合う競合関係にあるRNAを指す。mRNA、異なる種類のceRNA、miRNAは、ceRNAネットワークと呼ばれる相互作用のネットワークを形成している>。
一般に、miRNAは比較的安定した分子で、半減期が長いと考えられており、一般的な mRNAの約2~20倍長い。これと、それらの高い生産量を組み合わせることで、それらの細胞内存在量の高さとmRNA標的化における有効性が説明できる。
6.細胞外マイクロRNA:診断、予後、治療におけるバイオマーカー
循環マイクロRNA(circulating microRNA:c-miRNA)は、がん細胞が血流に放出される際に一緒に放出されるmiRNAで、がんの進行や転移に関与している可能性がある。
がんの診断、予後、治療における新しいバイオマーカーである[102]。ほぼすべての体液中に存在するc-miRNAは、さまざまな疾患(腫瘍性疾患、心血管疾患、神経変性病理など)の有望な高感度バイオマーカーであり、そのシグネチャは体の状態を正確に反映する。miRNAマーカーの発現に関する研究では、臨床症状が現れる前までに幅広い疾患を診断できること、また治療に対する患者の反応を評価して治療を修正および個別化できることが示され、外因性miRNAは、これらを目的とした診断および高精度治療薬として使用できる生体分子群の一つと結論付けられている[103][104][105]。表2にがん細胞とその隣接細胞の間を行き来する細胞外miRNAの概要を一覧化した。
表2 がん細胞とその隣接細胞の間を行き来する細胞外miRNA
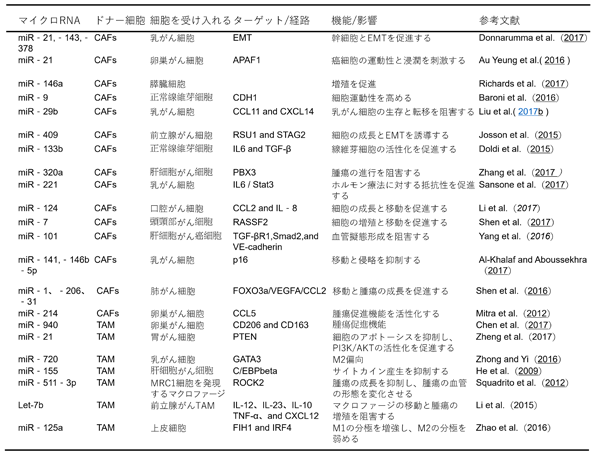
Bayraktar R et al., Mol Oncol. 2017 Dec;11(12):1673-1686 より引用し改変.
がんに関連するmiRNAの例としては、
miR-141, miR-200c, miR-196a, miR-203, miR-200a, miR-200b, miR-32, miR-375, miR-31, 及び miR-193aなどがある。また、表3に診断が難しいがんを検出するための臨床バイオマーカーとしての循環miRNAを示した[106]。
表3 診断が難しいがんを検出するための臨床バイオマーカーとしての循環 miRNA
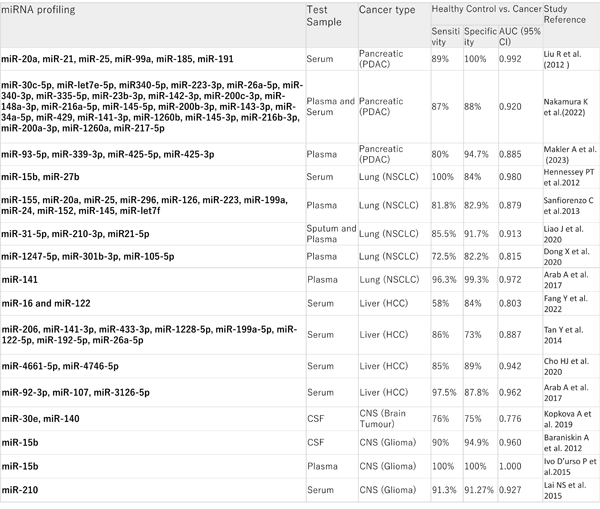
miR マイクロRNA、AUC 曲線下面積、PDAC 膵管腺癌、NSCLC 非小細胞肺癌、HCC 肝細胞癌、CSF 脳脊髄液、CNS 中枢神経系。
Metcalf GAD; Oncogene. 2024 Jul;43(28):2135-2142. を引用し、一部改変
いずれの報告でも特異性、感度は高いものの同じ臨床材料を用いた同じがんタイプの診断でも、診断に必要なmiRNAのプロファイリングの数や種類が異なる。これは、今後の研究課題として解決が求められるところでもある。診断目的を明確化して用いないと結果に誤りを招く可能性も否定できない。
各種疾患のバイオマーカーとしてのmiRNAは、前述の標準的なmiRNAの生合成経路に対し非標準的経路により生合成されるものもある。非標準的経路は主にDrosha、Dicer、エクスポーター5、およびAGO2など、標準的な経路に関与するタンパク質をすり抜けるなど、さまざまな組み合わせを利用する。一般に、非標準的なmiRNA生合成は、Drosha/DGCR8非依存経路とDicer非依存経路に分類される。図5にA:標準的な生合成経路を対象に、B:Drosha非依存経路、C:snoRNA由来経路、D:XPO5非依存経路、E:Dicer非依存経路を図示した[107]。
7.真のヒトmiRNAの総数の推定[52]
『ヒトのmiRNA候補の数は増加の一途をたどっているが、完全に特性決定され、実験的に検証されているものはごくわずかである。真のmiRNAの総数を決定するために、我々はインシリコによる高スループットと実験による低スループットを組み合わせた検証戦略、を採用した。我々は、3,637億のシーケンシングリードを含む28,866のヒトsmall RNAシーケンシングデータセットを収集し、誤って注釈されたデータや低品質なデータは除外した。ハイスループット解析の結果、24,127の成熟miRNA候補の65%が偽陽性である可能性が高いと同定された。ノーザンブロッティングを用いて、miRBaseに登録されたmiRNAと新規miRNA候補を実験的に検証した。205の成熟miRNAをコードする108の前駆体を外因性過剰発現させることで、miRBaseエントリーの68.5%を確認し、高信頼性エントリーの確認率は94.4%、新規miRNA候補の確認率は18.3%に達した。内因性miRNAの解析では、12種類のヒト細胞株で8種類のmiRNAの発現を確認した。合計で2,300の真のヒト成熟miRNAが推定され、そのうち1,115は現在miRBase V22に注釈されている。実験的に検証されたmiRNAは、誤って注釈されたmiRNAを利用して仮説化されたターゲットオームを修正することに貢献するだろう。文献[52]のAbstractをDeepL.com(無料版)で翻訳』
『ヒトゲノムは1,900以上のmiRNAをコードしている可能性がある[108][109]。しかし、手動でキュレーションされたmiRNA遺伝子データベースMirGeneDBで本物のmiRNAを表すヒトmiRNAは約500個だけである[110]。microRNA Wikipedia: microRNA - Wikipediaより抜粋し和訳』
8.マイクロRNAのSNPとisomiR
1) miRNAのSNPs(Single Nucleotide Polymorphisms)
SNPsは、miRNAの遺伝子配列における単一ヌクレオチドの変異です。これにより、miRNAの配列が変わり、その結果、miRNAの機能や結合パートナー(ターゲットRNA)に影響を与えることがある。SNPsは、miRNAの発現や生物学的役割に関連する疾患のリスク因子としても注目されている[111]-[114]。
2) isomiRs(isomiRs)
isomiRsは、基準配列に対して変異を持つmiRNA配列です。miRNAの自然なバリエーションであり、miRNAのプロセシング過程で生じる多様性を指す。これには、miRNAの5'末端や3'末端の修飾、スプライシングによるアイソフォームの生成などが含まれる。isomiRsは、miRNAの機能やターゲットRNAへの結合特性に影響を与えることがある[115]。
<miRNAのSNPsとisomiRsの違い>
- ●SNPsは遺伝子レベルの変異であり、miRNAの配列に直接影響を与える。
- ●isomiRsはmiRNAのプロセシング過程で生じるバリエーションであり、miRNAの構造や機能に影響を与える可能性がある[116][117]。
どちらもmiRNAの機能に重要な役割を果たすが、SNPsは遺伝的な変異、isomiRsはプロセシングによる多様性という違いがある。
ⅰ. isomiRsの種類
isomiRsは、miRNAのプロセシング過程で生じるバリエーションであり、主に以下のような種類がある:
- a.5'末端の修飾:DroshaやDicerの切断部位がmiRNAの5'末端に対して上流または下流にずれることにより、5'末端が異なるisomiRsが生じる。
- b.3'末端の修飾:Dicerの切断部位がmiRNAの3'末端に対して上流または下流にずれることにより、3'末端が異なるisomiRsが生じる。
- c.3'末端のヌクレオチド添加:miRNAの3'末端にヌクレオチドが追加されることにより、新しいisomiRsが生じる。
- d.ヌクレオチド置換:miRNAの前駆体の配列に変異が生じ、その結果として異なるisomiRsが生じる。
表4にハイスループット小分子RNAシーケンシングによって決定されたmiRNA変異体の発現例を示した。Canonical(標準的な、正統な)に対し4つのisomiR variantを示した。
表4 ハイスループット小分子RNAシーケンシングによって決定された miR 変異体の発現例
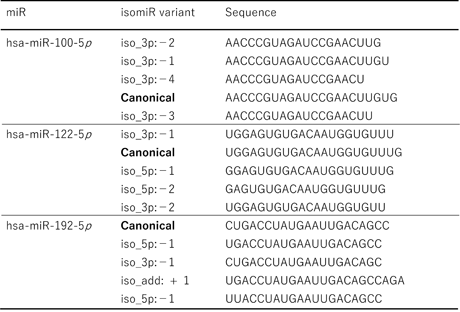
Franco S, Pluvinet R, et al., Sci Rep. 2022 Oct 14;12(1):17220.より引用し改変
ⅱ. isomiRsの機能
isomiRsは、miRNAの安定性、細胞内局在、ターゲット選択に影響を与えることがある。例えば、3'末端のヌクレオチド添加はmiRNAの安定性を変化させることがあり、異なるターゲットRNAと結合する可能性がある[118]-[122]。
ⅲ. isomiRsの研究
isomiRsは、次世代シーケンサーを用いたRNAディープシーケンシング技術の進歩により増加傾向にある。これに伴い、マイクロRNAファミリーの拡大と共に多様性とその生物学的役割についての理解も深まっている。
isomiRsは、miRNAのプロセシング過程で生じるバリエーションであり、miRNAの機能やターゲット選択に影響を与えることがある。さまざまな種類のisomiRsが存在し、それぞれ異なる生物学的役割を持つ可能性がある。
9.エクソソームマイクロRNA Exosomal microRNA(exomiR)
エクソソームマイクロRNA(exomiR)は、エクソソームに含まれる小さな非コードRNA分子です。エクソソームは細胞から放出され、細胞間でさまざまな分子を運ぶ小さな小胞です。エクソソーム(Exosome)とは、細胞から放出されるエンドサイトーシス起源の直径30~150ナノメートルの細胞外小胞(Extracellular vesicle)の一種で、細胞膜と同じ二重の脂質膜でできており、内部には核酸(マイクロRNA、メッセンジャーRNA、DNAなど)やタンパク質などの生体物質を内包している。図6にエクソソームの構造と内容を示した。
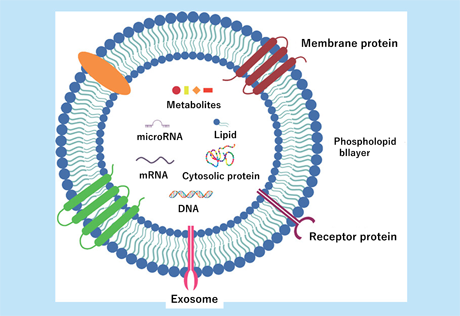
図6 エクソソームの構造と内容
Dilsiz N., Future Sci OA. 2020 Feb 26;6(4):FSO465. より引用
細胞から分泌されたエクソソームは生体液(血液、髄液、尿など)を循環し、他の細胞に運ばれる。細胞に吸収されたエクソソーム中の物質がその細胞内で働くことで、細胞に影響を与える。エクソソームの内包物であるmiRNAは特に、がんや心臓病、糖尿病など、さまざまな疾患への関与が示され、細胞間コミュニケーションに重要な役割を果たしている。図7にmiRNA排出メカニズムと細胞外生存を示した。miRNAは多小胞体(MVB)やエクソソームを介した細胞排出、膜剥離による微小小胞形成、AGO-2やHDLとの関連など、さまざまな方法を通じて細胞から能動的および受動的に放出される。
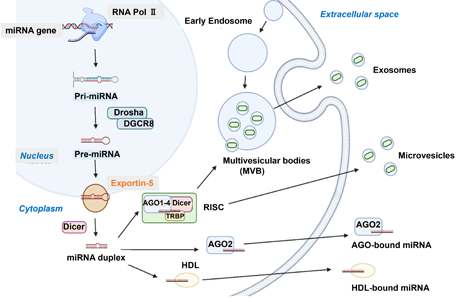
図7 miRNA排泄メカニズムと細胞外生存
Metcalf, G.A.D; Oncogene 43, 2135–2142 (2024).より引用
循環miRNAの区画化:循環miRNAは、小胞(エクソソーム、微粒子、アポトーシス小体)、タンパク質複合体(Ago2、NPM1)、およびリポタンパク質複合体(HDL、LDL 複合体)に内包もしくは結合状態で存在する。
哺乳類細胞は、エクソソーム、微小小胞、アポトーシス小体など、さまざまな種類の細胞外小胞(EV)を放出する。これらの放出されたEVは、全身を循環する生体液と共に循環し、もしくは排出する生体液と排出される[123]。
miRNAは産生細胞だけで無く、近接さらには遠位細胞や組織にも到達し、作用を発揮する。細胞間コミュニケーションに参加するmature-miRNAは、多くの場合EV内でほとんどの細胞から放出され、細胞外液を介して拡散して腫瘍細胞などの遠隔標的細胞に到達する。腫瘍細胞の表現型は、標的に応じて腫瘍抑制因子またはがん遺伝子としてmRNAとタンパク質の発現を制御することによって影響を受ける。このエクソソームに含有するmiRNAを分析・解析し、診断・治療へのバイオマーカーとして活用する研究が活況である[124]。
10.まとめ
- ●DNAから転写されたRNAで、タンパク質に翻訳されないRNAをncRNAと総称する。
- ●ncRNAは、制御性ncRNAとハウスキーピングncRNAに群別され、制御性ncRNAは、200ntを境に小分子(短鎖)と高分子(長鎖)非コードRNAに分ける。
- ●小分子非コードRNAには、miRNA、siRNAが長鎖非コードRNAにはlncRNAとしてXist、HOTAIRや環状RNAなどがある。
- ●miRNAは短鎖ncRNAの一群で17~24ntの一本鎖RNAで、RISCに取込まれて機能する。
- ●miRNAは、mRNAの転写産物の相補配列と部分的に結合し、mRNAの翻訳を阻害することでターゲットmRNAのタンパク質発現を抑制する。
- ●miRNAは、がん、心血管疾患、神経変性疾患など多くの疾患の診断や予後のバイオマーカーおよび治療に用いられる。
【miRNAによる翻訳抑制の仕組み】
- ●miRNAは単独では機能を発現できない。RNA-タンパク質複合体であるRISCを形成し機能を発現する。
- ●miRNAは、標的mRNAの3'-非翻訳領域に結合する。
- ●miRNAは、標的mRNAの翻訳開始の段階を阻害する。
- ●miRNAは、翻訳開始因子eIF4Aを標的mRNAから特異的に解離させることで、リボソームの呼び込みを阻害する。
【細胞外および循環miRNA】
- ●生体液中には、細胞外 miRNAとしてエクソソームなどの小胞に内包され、もしくはタンパク質、特に AGO2 と接合して血液などと循環するものがある。細胞外 miRNA に接合するタンパク質には、HDL やNPM1 、アルブミンなどがある。
- ●miRNAは、エクソソームなどの小胞に内包もしくはAGO2と結合したものは安定であるが、種類、形状他の因子により安定性が大きく異なるため充分な調査が望まれる。
【循環腫瘍マイクロRNAの働き】
- ●がん細胞が血流に放出される際に、特定のmiRNAも同時に放出される。このmiRNAはCTCの生存や転移能力を高める役割を果たしていると考えられている。
- ●CTCと循環腫瘍マイクロRNAは協力してがんの転移を促進する可能性がある。
【miRNAのバリアント】
- ●SNPsは遺伝子レベルの変異であり、miRNAの配列に直接影響をおよぼす。
- ●miRNAには、末端の1または2塩基が異なる多型(isomiRs)がしばしばみられる。isomiRsは、miRNAのプロセシング過程で生じるバリエーションであり、miRNAの機能やターゲット選択に影響を与えることがある。さまざまな種類のisomiRsが存在し、それぞれ異なる生物学的役割を持つ可能性があり研究は継続している。
- ●isomiRsは、次世代シーケンサーを用いたRNAディープシーケンシング技術の進歩により増加傾向にある。
マイクロRNA(miRNA)は、長さが約19~25nt(サイズは筆者によりバリアント類の捉え方で若干異なる)の小さな非コードRNAで、さまざまな標的遺伝子を制御するため、がんの形成と発達を含むさまざまな生物学的プロセスと病理学的プロセスの制御に関与している。がん化学療法における薬剤耐性は、この悪性疾患の治療における主な障害の1つである。統計データによると、がん患者の死亡率の90%以上が薬剤耐性に関連している。がん化学療法の薬剤耐性は、抗腫瘍薬の取り込みの低下、薬物標的の変更、細胞周期チェックポイントの変化、DNA損傷修復の増加など、多くのメカニズムによって引き起こされる可能性がある。近年、多くの研究で、miRNAが薬剤耐性関連遺伝子を標的にしたり、細胞増殖、細胞周期、アポトーシスに関連する遺伝子に影響を与えたりすることで、腫瘍細胞の薬剤耐性への関与が示唆されている[125]。さらに議論の余地は有るが食事性エピジェネティック調節因子としてのmiRNAの関与も解決すべき課題である[126]。
おわりに
諸種疾患の発動初期の診断、治療診断、予後診断さらには診断困難であった疾患群の診断にと期待が膨らむncRNA分析分野である。しかし、期待だけで猛進しては真価を生みそびれる事も念頭に抱く必要がある。たしかに臨床において夢を抱ける分子群であるが、それゆえの慎重さも必要と思われる。多大な研究結果が産出されている今の時期に、分析を担うであろう臨床検査部門を担当する者は、この分子群の知識・技術への洽覧深識が必然的に求められる。さらには、AIを含む機械学習に関しても見識を深めるべきである。結果として、疾患罹患者の待望する、発症の低減化と完治をめざした医療の進展を大きく牽引できるかもしれない。現時点では、分析・解析に高価な機器の使用や高度な分析技術が求められるが、現状の設備でも体制の構築により一歩ずつ歩みを進めることは可能と思われる。本稿が近付きつつある理想郷に踏み出す糧になれれば幸いである。
参考文献・資料
- Carninci P, et al. Science 309(5740):1559–1563.
- Hangauer MJ, et al., PLoS Genet 9(6):e1003569.
- Rinn J.L., et al. Annu. Rev. Biochem. 2012;81: 145–166.
- Dhanoa J.K., et al., Hanguk Tongmul Chawon Kwahakhoe Chi. 2018;60:25.
- Mattick, J. Nat Rev Genet 5, 316–323 (2004).
- Gagen, M.J., Theory Biosci. 123, 381–411 (2005).
- Dawoud A, et al. Noncoding RNA Res. 2022 Oct 12;8(1):60-74.
- Pamudurti NR, et al. (April 2017). Molecular Cell. 66 (1): 9–21.e7.
- Loganathan T, Funct Integr Genomics. 2023 Jan 10;23(1):33.
- Elbashir S.M. et al., Nature. 2001;411:494–498.
- Galasso, M., Genome Med 2, 12 (2010).
- Beňačka, R. et al. Int. J. Mol. Sci. 2023, 24, 16213.
- Faehnle C.R., Curr. Opin. Chem. Biol. 2007;11:569–577.
- Matera A.G., et al., Nat. Rev. Mol. Cell Biol. 2007;8:209–220.
- Christov C.P., et al., Mol. Cell. Biol. 2006; 26:6993–7004.
- Christov C.P. et al., Br. J. Cancer. 2008; 98:981–988.
- Fernandes JCR, et al., Noncoding RNA. 2019 Feb 17;5(1):17.
- Ma L, et al., Nucleic Acids Res. 2019 Jan 8;47(D1): D128-D134.
- Cabili, M.N. et al. Genes Dev. 2011, 25, 1915–1927.
- Li, K., Oncotarget. 2010, 1, 447–452.
- Zhao N, et al. Apoptosis. 2024 Oct;29(9-10):1584-1599.
- Non-coding RNA: Non-coding RNA - Wikipedia
- Wu, YY., J Biomed Sci 27, 49 (2020).
- Ledford H. Nature. 2013 Feb 28;494(7438):415.
- Seimiya T, et al., J Hum Genet. 2021 Feb;66(2):181-191.
- Kalogianni DP, et al., Anal Bioanal Chem. 2018 Jan;410(3):695-713.
- Henke JI, et al., EMBO J. 2008;27:3300–3310.
- Ma C, et al., Sci China C Life Sci. 2009 Apr;52(4):323-30.
- Turchinovich A, et al. Trends Biochem Sci. 2012;37:460–465.
- Ghosh Z, et al., Biochem Biophys Res Commun. 2007 Nov 9;363(1):6-11.
- Vincent C. et al., Cell. 2013 February 14; 152(4): 844–858.
- Y. Lee, et al., EMBO J, 21 (2002), pp. 4663–467.
- XUEZHONG CAI, et al., RNA (2004), 10:1957–1966.
- Murchison EP, Curr Opin Cell Biol. 2004 Jun;16(3):223-9.
- Pratt AJ, J Biol Chem. 2009 Jul 3;284(27):17897-901
- Filipowicz W, et al. Nat Rev Genet. 2008 Feb;9(2):102-14
- Wakiyama M, et al. Genes Dev. 2007 Aug 1;21(15):1857-62.
- Preall JB, Cell. 2005 Nov 18;123(4):543-5.
- RNA interference - a comprehensive overview:RNA interference overview | Abcam1
- Siomi H, Nature. 2009 Jan 22;457(7228):396-404.
- Preall JB, et al. Curr Biol. 2006 Mar 7;16(5):530-5.
- Kawamata T, et al., Nat Struct Mol Biol. 2009 Sep;16(9):953-60.
- Santhekadur PK, Genes Dis. 2019 Sep 17;7(2):199-204.
- Lewis B.P., et al., Cell. 2003; 115:787–798.
- Hibio N, et al., Sci Rep. 2012;2:996.
- Griffiths-Jones S, et al., Nucleic Acids Res. 2008 Jan;36(Database issue):D154-8.
- Ambros V, et al. RNA. 2003 Mar;9(3):277-9.
- WikipediaマイクロRNA:miRNA - Wikipedia
- Meštrović, Tomislav. 2023. News-Medical, viewed 08 January 2025, https://www.news-medical.net/life-sciences/MicroRNA-Nomenclature.aspx.
- Desvignes T, et al., Trends Genet. 2015 Nov;31(11):613-626.
- Clustered Ref SNPs (rs) and Other Data Computed in House
- Alles J, et al., Nucleic Acids Res. 2019 Apr 23;47(7):3353-3364.
- Bartel DP. Cell. 2009 Jan 23;136(2):215-33.
- Bartel DP. Cell. 2018 Mar 22;173(1):20-51
- Jonas S, Nat Rev Genet. 2015 Jul;16(7):421-33.
- Guo H, et al., Nature. 2010 Aug 12;466(7308):835-40.
- Kawamata T, Trends Biochem Sci. (2010) 35:368–76.
- Jo MH, et al., Mol Cell. (2015) 59:117–24.
- Krützfeldt J, et al. Nature (2005) 438:685–9.
- Ameres SL, et al. Science (2010) 328:1534–9.
- Xu W, et al. BMC Bioinformatics. 2014;15 Suppl 7(Suppl 7):S4.
- Ellwanger DC, et al., Bioinformatics (2011) 27:1346–50.
- Richard W. et al. Cell, Volume 136, Issue 4, 20 February 2009, Pages 642–655.
- Lim LP, et al. Nature. 2005 Feb 17;433(7027):769-73. Epub 2005 Jan 30.
- Schmitz U, et al., Nucleic Acids Res. 2014 Jul;42(12):7539-52.
- Valadi H, et al. Nat. Cell Biol. 9, 654–659 (2007).
- Mitchell PS, et al. Proc. Natl. Acad. Sci. USA 105, 10513–10518 (2008).
- Capobianco V, et al. J. Proteom. Res. 11, 3358–3369 (2012).
- Samanta S, et al. Acta Pharmacol Sin. 2018 Apr;39(4):501-513.
- Gallo A, et al. PLoS ONE (2012) 7: e30679.
- Turchinovich A, et al. Nucleic Acids Res. (2011) 39:7223–33.
- Vickers KC, et al. Nat Cell Biol. (2011) 13:423–33
- Tabet F, et al. Nat Commun. (2014) 5:3292.
- Wang K, et al. Nucleic Acids Res. (2010) 38:7248–59.
- Arroyo JD, et al. Proc Natl Acad Sci USA (2011) 108:5003–8.
- Botti V, et al., Int J Mol Sci. 2022 Jan 24;23(3):1291.
- Kosaka N, et al. J Biol Chem. 2013;288:10849–10859.
- Frank F, et al. Nature. 2010; 465:818–822.
- Koppers-Lalic D, et al. Cell Rep. 2014;8:1649–1658.
- Barman B, J Biol Chem. (2015) 290:24650–6.
- Nishi K, et al. Nucleic Acids Res (2015) 43:9856–73.
- Detzer A, et al., Nucleic Acids Res. (2011) 39:2727–41.
- Bose M, et al., Mol Cell Biol. (2017) 37:e00464–16.
- Gibbings DJ, et al., Nat Cell Biol. (2009) 11:1143–9.
- Zhang X, et al. Cell (2014) 158:607–19.
- Barrey E, et al., PLoS ONE (2011) 6:e20220.
- Gagnon KT, et al., Cell Rep. (2014) 6:211–21.
- Miao L, et al. Biochim Biophys Acta (2016) 1859:650–62.
- Delihas N. World J Biol Chem. 2015 Nov 26;6(4):272-80.
- Iftikhar H, Bioessays ( 2016) 38:367–78.
- Kosaka N, et al. J Biol Chem (2010) 285:17442–52.
- Chen X, et al. Trends Cell Biol. (2012) 22:125–32.
- Aucher A, et al, J Immunol. (2013) 191:6250–60
- O'Brien J, et al., Front Endocrinol (Lausanne). 2018 Aug 3;9:402.
- Chen X, et al. Cell Res (2008) 18:997–1006.
- Cogswell JP, et al. J Alzheimers Dis. (2008) 14:27–41.
- Zhou Q, et al. Int J Biol Sci (2012) 8:118–23.
- Weber JA, et al. Clin Chem. (2010) 56:1733–41.
- da Silveira JC, et al., Biol Reprod. (2012) 86:71.
- Marzi MJ, et al. Genome Res. 2016 Apr;26(4):554-65.
- Oikawa S, et al. FEBS J. 2023 Dec;290(24):5692-5703.
- Allegra A, et al., Int J Oncol. 2012 Dec;41(6):1897-912.
- Ramzan F, et AL. Acta Diabetol. 2020 Feb;57(2):203-214.
- Bayraktar R, et al. Mol Oncol. 2017 Dec;11(12):1673-1686.
- Pozniak T, et al. Int J Mol Sci. 2022 Apr 3;23(7):3996.
- Metcalf GAD. Oncogene. 2024 Jul;43(28):2135-2142.
- Gregorova J, et al. Cancers (Basel). 2021 Mar 16;13(6):1333.
- "Homo sapiens miRNAs". miRBase. Manchester, UK: Manchester University.
- Li M, et al. World J Surg. 2009 Apr;33(4):667-84.
- Fromm B, et al., Nucleic Acids Res. 2020 Jan 8;48(D1): D132-D141.
- Gong J, et al., Hum Mutat. 2012 Jan;33(1):254-63.
- Teruel-Montoya R, et al.,2015 Feb;13(2):170-81.
- Katayama K, et al., Noncoding RNA Res. 2021 Jun 27;6(3):123-129.
- Wang F, et al., Am J Med Sci. 2021 Jul;362(1):5-12.
- Morin RD, et al., Genome Res. 2008 Apr;18(4):610-21.
- Loher P, et al., Oncotarget. 2014 Sep 30;5(18):8790-802.
- Neilsen CT, et al., Trends Genet. 2012 Nov;28(11):544-9.
- Lausten MA, Noncoding RNA. 2023 Jun 7;9(3):34.
- Bofill-De Ros X, et al., Biochim Biophys Acta Gene Regul Mech. 2020 Apr;1863(4) : 194373.
- Tan GC, Malays J Pathol. 2015 Aug;37(2):73-81.
- Glogovitis I, et al., Biomolecules. 2020 Dec 30;11(1):41.
- Tomasello L, et al., Front Cell Dev Biol. 2021 Jun 9;9:668648.
- Rahimian N, et al. Methods Mol Biol. 2023;2595:13-47.
- Cao D, et al. Hematol Oncol. 2022 Apr;40(2):172-180.
- Si W, et al. Clin Epigenetics. 2019 Feb 11;11(1):25.
- Martino E, et al. Nutrients. 2024 Jan 3;16(1):160.
2025.07